用氯气消毒的水常有异味,长期食用氯气处理过的食物可能导致人体摄自食物的不饱和脂肪酸活性减弱,产生活性毒素,对人造成潜在危害。约从40年代起,国外就有用ClO2来消毒饮用水的。ClO2是一种广谱型的消毒剂,根据世界环保联盟的要求,ClO2将逐渐取代Cl2,成为生产自来水的消毒剂。工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得,在这个反应中NaClO3和Na2SO3的物质的量之比为
| A.1∶1 | B.2∶1 | C.1∶2 | D.2∶3 |
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是
| 选项 |
叙述Ⅰ |
叙述Ⅱ |
| A |
溶解度:Na2CO3>NaHCO3 |
向饱和的Na2CO3溶液中通入CO2,析出白色晶体 |
| B |
CaSO3是难溶物 |
向CaCl2溶液中通入SO2产生白色沉淀 |
| C |
NH3能使酚酞溶液变红 |
NH3可用于设计喷泉实验 |
| D |
强酸可与碱及弱酸盐反应 |
用硫酸清洗锅炉中的水垢 |
下列各组物质中,满足表中图示物质在通常条件下能一步转化的组合只有
| 序号 |
X |
Y |
Z |
W |
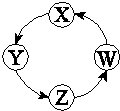 |
| ① |
Cu |
CuSO4 |
Cu(OH)2 |
CuO |
|
| ② |
Na |
NaOH |
Na2CO3 |
NaCl |
|
| ③ |
Cl2 |
Ca(ClO)2 |
HClO |
HCl |
|
| ④ |
Fe |
FeCl3 |
FeCl2 |
Fe(OH)2 |
A.①②③B.①③④C.②③D.①②④
某化学小组在常温下测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:
方案Ⅰ:铜铝混合物 测定生成气体的体积
测定生成气体的体积
方案Ⅱ:铜铝混合物 测定剩余固体的质量
测定剩余固体的质量
下列有关判断中不正确的是
| A.溶液A和B均可以是盐酸或NaOH溶液 |
| B.溶液A和B均可以选用稀硝酸 |
| C.若溶液B选用浓硝酸,则测得铜的质量分数偏小 |
| D.实验室方案Ⅱ更便于实施 |
实验室用碳酸钠晶体配制1.00mol/L的Na2CO3溶液100mL,造成所配溶液浓度偏低的原因是
| A.暴露在空气中称量碳酸钠晶体(Na2CO3•10H2O)的时间太长 |
| B.向容量瓶转移液体时,容量瓶事先用蒸馏水洗涤 |
| C.定容时俯视刻度线 |
| D.称量碳酸钠晶体(Na2CO3•10H2O)的烧杯未干燥 |
一定温度下,向饱和NaOH溶液中加入一定量的钠块,充分反应后恢复到原来温度,下列说法正确的是
| A.溶液中溶质质量增加,溶剂质量减少,溶液中溶质的质量分数变大 |
| B.溶液的pH不变,有氢气放出 |
| C.溶液中的Na+数目减小,有氧气放出 |
| D.溶液中的c(Na+)增大,有氢气放出 |