如图所示,在蒸发皿中放一小块钠,加热至熔化时,用玻璃棒蘸取少量无水CuSO4与熔化的钠接触,瞬间产生耀眼的火花,同时有红色物质生成。据此判断下列说法中不正确的是( ) 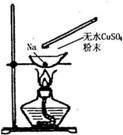
| A.上述反应是置换反应 |
| B.上述反应是放热反应 |
| C.上述反应中CuSO4表现了还原性 |
| D.加热且无水条件下,Na可以与CuSO4反应并生成Cu |
A、B、C是三种金属,根据下列①、②两个实验:①将A与B浸在稀硫酸中用导线相连,A上有气泡逸出,B逐渐溶解;②电解物质的量浓度相同的A2+、C2+盐溶液时,阴极上先析出C(使用惰性电极)。确定它们的还原性强弱顺序为
A.A>B>C B.B>C>A C.C>A>B D.B>A>C
下列电离方程式书写不正确的是
A.2H2O H3O++OH- H3O++OH- |
B.H2S H+ + HS- H+ + HS- |
C.NaHS Na++HS- Na++HS- |
D.NaHCO3 = Na+ + HCO3- |
反应A(g)+3B(g) 2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是
2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是
A.υ(D)="0.4" mol ·L-1·s-1B.υ(C)="0.5" mol ·L-1·s-1
C.υ(B)="0.6" mol ·L-1·s-1D.υ(A)="0.15" mol ·L-1·s-1
下列变化过程中,△S<0的是
| A.氯化钠溶于水中 | B.NH3(g)与HCl(g)反应生成 NH4Cl(s) |
| C.干冰(CO2)的升华 | D.CaCO3(s)分解为CaO(s)和CO2(g) |
在中和热测定的实验中不需要用到的仪器是
| A.量筒 | B.温度计 | C.环形玻璃搅拌棒 | D.天平 |