对于可逆反应 ,下列叙述正确的是
,下列叙述正确的是
| A.达到化学平衡状态时,4v正(O2)=5v逆(NO) |
| B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到化学平衡状态 |
| C.达到化学平衡状态后,若增大容器容积,则正反应速率减小,逆反应速率增大 |
| D.化学反应速率的关系为2v正(NH3)=3v正(H2O) |
立方烷(C8H8)、棱晶烷(C6H6)是近年来运用有机合成的方法制备的具有如下图所示立体结构的环状有机物。萜类化合物是广泛存在于动、植物体内的一类有机物(例如盆烯、月桂烯、柠檬烯等)。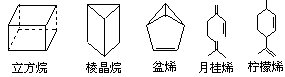
对上述有机物的下列说法中正确的是
①盆烯、月桂烯、柠檬烯都能使溴水褪色②棱晶烷、盆烯、与苯互为同分异构体③月桂烯、柠檬烯互为同分异构体④立方烷、棱晶烷是环烷烃的同系物
| A.①②③ | B.①②④ | C.①③④ | D.②③④ |
在一定条件下,萘可以和硝酸、硫酸和混合酸发生硝化反应,生成二硝基物,它是1,5-二硝基萘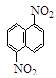 和1,8—二硝基萘
和1,8—二硝基萘 的混合物。后者可溶于质量分数大于98%的硫酸,而前者不能。利用这一可以将这两种异构体分离。将上述硝化产物加入适量的98.3%硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中得到固体1,8—二硝基萘,应采用方法是
的混合物。后者可溶于质量分数大于98%的硫酸,而前者不能。利用这一可以将这两种异构体分离。将上述硝化产物加入适量的98.3%硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中得到固体1,8—二硝基萘,应采用方法是
| A.对所得的滤液蒸发、浓缩、冷却、结晶 | B.向滤液中缓缓加入水后过滤 |
| C.向滤液中加入Na2CO3溶液后过滤 | D.将滤液缓缓加入水中后过滤 |
图中所示化合物A(fumimycin)是从微生物中分离得到的,它显示出广谱抗菌活性。下列关于化合物A的说法中,正确的是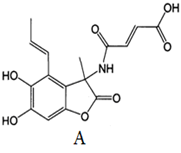
| A.该化合物A的分子式为:C15H15O6N |
| B.化合物A可以水解得到2种有机物 |
| C.化合物A可以与 H2发生加成反应,1mol A最多消耗H2 2mol |
| D.化合物A与足量的溴水反应,2mol A可以消耗5mol Br2 |
以纯锌作阴极,以石墨作阳极,电解某浓度的硫酸锌溶液,阴极产物均附在电极上,通电一段时间后,关闭电源,迅速撤去电极(设阴极产物没有损耗),若在电解后的溶液中加入4.95g Zn(OH)2固体,则恰好能使溶液恢复到原浓度,则整个电解过程中,所产生的气体总体积为(标准状况)
| A.0.56L | B.1.12L | C.2.24L | D.3.36L |
最新研发的波音787客机具有更省油、更舒适的特点,波音787还是首款使用碳纤维复合材料超过50%的客机,开创了在航空航天领域复合材料大范围代替传统金属的新时代。下图所示的某聚酰胺树脂是波音飞机材料中的一种,具有较好的耐热性、耐水性。则下列说法正确的是
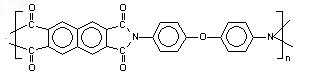
| A.碳纤维复合材料中,碳纤维是增强材料,该树脂是基体材料 |
| B.复合材料是未来材料发展的趋势,因此应该停止金属材料的研究 |
| C.该树脂中所有原子共平面 |
D.该树脂可以由单体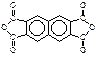 和 和 通过加聚反应得到 通过加聚反应得到 |