今有HA、H2B两种弱酸,有如下关系:H2B+A-=HB-+HA B2-+HA=HB-+A-则下列说法正确的是:
A、H2B的电离方程式为:H2B 2H+ + B2-
2H+ + B2-
B、结合质子能力由强到弱的顺序为:B2->A->HB-
C、等物质的量浓度NaA、NaHB、Na2B三种盐的水溶液,NaA碱性最强
D、等pH的HA、H2B两种溶液中,水的电离出的氢离子前者大于后者
用下列实验装置进行相应实验,能达到实验目的的是(夹持装置未画出)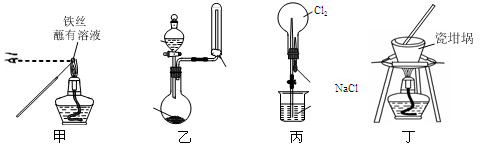
| A.用装置甲检验溶液中是否有K+ |
| B.用装置乙制取并收集少量NH3 |
| C.用装置丙进行喷泉实验 |
| D.用装置丁加热熔融NaOH固体 |
下列物质性质与应用对应关系正确的是
| A.浓硫酸具有脱水性,可用于干燥CO2 |
| B.氨气具有还原性,可用于检查HCl泄漏 |
| C.四氯化碳密度比水大,可用于萃取溴水中的Br2 |
| D.氧化铝具有高熔点,可用于生产耐火砖 |
下列有关化学用语表示正确的是
A.过氧化钙(CaO2)的电子式: |
B. 离子的结构示意图: 离子的结构示意图: |
C.H2CO3的电离方程式:H2CO3 2H++CO32- 2H++CO32- |
| D.葡萄糖的结构简式:C6H12O6 |
国务院颁布的《“十二五”控制温室气体排放工作方案》提出,2015年我国单位国内生产总值CO2排放要比2010年下降17 %。下列说法不正确的是
| A.CO2属于酸性氧化物 |
| B.CO2是导致酸雨发生的主要原因 |
| C.可用Na2CO3溶液捕捉(吸收)CO2 |
| D.使用氢能源替代化石燃料可减少CO2排放 |
用一种阴、阳离子双隔膜三室电解槽处理废水中的NH4+,模拟装置如图所示。下列说法正确的是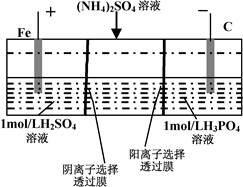
| A.阳极室溶液由无色变成棕黄色 |
| B.阴极的电极反应式为:4OH–-4e–=2H2O+O2↑ |
| C.电解一段时间后,阴极室溶液中的pH升高 |
| D.电解一段时间后,阴极室溶液中的溶质一定是(NH4)3PO4 |