常温下Ksp(AgCl)=1.56×10-10, Ksp(AgI)=1.0×10-16,将等体积的AgCl和AgI的饱和溶液的清夜混合,再向其中加入一定量的AgNO3固体,下列说法正确的是
| A.两清夜混合,AgCl和AgI都沉淀。 |
| B.向AgCl清夜加入AgNO3固体,c(Ag+)增大,Ksp(AgCl)也增大 |
| C.若AgNO3固体足量,AgCl和AgI都可沉淀,但以AgCl沉淀为主 |
| D.若取0.235克AgI固体放入100ml(忽略体积变化),c(I-)=0.01mol/l |
已知:(1)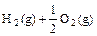 =H2O(g)△H1=a kJ·
=H2O(g)△H1=a kJ·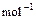
(2)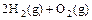 =2H2O(g)△H2=b kJ·
=2H2O(g)△H2=b kJ·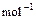
(3)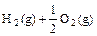 =H2O(l)△H3=c kJ·
=H2O(l)△H3=c kJ·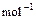
(4)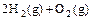 =2H2O(l)△H4=d kJ·
=2H2O(l)△H4=d kJ·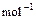
下列关系式中正确的是()
| A.a<c <0 | B.b>d>0 | C.2a=b<0 | D.2c=d>0 |
下列说法不正确的是( )
| A.需要加热才能发生的反应不一定是吸热反应 |
| B.任何放热反应在常温条件下一定能发生反应 |
| C.反应物和生成物所具有的总能量决定了反应放热还是吸热 |
| D.吸热反应在一定条件下(如常温、加热等)也能发生反应 |
CO和H2在一定条件下可以合成乙醇:2CO(g)+4H2(g) CH3CH2OH(g)+H2O(g),下列叙述中能说明上述反应在一定条件下已达到最大限度的是()
CH3CH2OH(g)+H2O(g),下列叙述中能说明上述反应在一定条件下已达到最大限度的是()
| A.CO全部转化为乙醇 |
| B.正反应和逆反应的化学反应速率均为零 |
| C.CO和H2以1∶2的物质的量之比反应生成乙醇 |
| D.反应体系中乙醇的物质的量浓度不再变化 |
下列关于物质的组成、性质或用途的叙述错误的是()
| A.可燃冰是一种天然气的水合物,它的开采使用有助于解决温室效应 |
| B.乙烯分子中的不饱和碳碳双键比乙烷分子中碳碳单键活泼,易于被加成 |
| C.煤的液化、气化可以提高经济效益,减少酸雨等环境危害的发生 |
| D.工业酒精含95%左右的乙醇,可以用于酒精饮料的勾兑,降低生产成本 |
关于下列图示的说法中正确的是()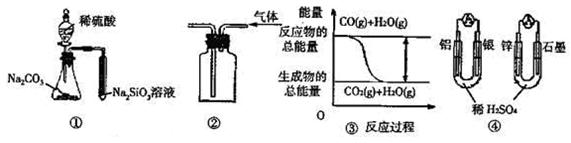
| A.用图①所示实验可比较硫、碳、硅三种元素的非金属性强弱 |
| B.用图②所示实验装置排空气法收集CO2气体 |
C.图③表示CO(g)+H2O(g) CO2(g)+H2(g)为吸热反应 CO2(g)+H2(g)为吸热反应 |
| D.图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量也相同 |