含6.02×1023个原子的氧气在标准状况下所占的体积是
| A.44.8 L | B.22.4 L | C.11.2 L | D.5.6 L |
下列判断正确的是:①任何物质在水中都有一定的溶解度②浊液用过滤的方法分离③分散系一定是混合物④丁达尔效应、布朗运动、渗析都是胶体的物理性质⑤同一种溶质的饱和溶液要比不饱和溶液浓些⑥布朗运动不是胶体所特有的运动方式⑦任何溶胶加入可溶性电解质后都能使胶粒发生聚沉⑧相同条件下,相同溶质的溶液,饱和溶液要比不饱和溶液浓些。
| A.③⑥⑧ | B.②④⑥⑧⑦ | C.①②③④⑤ | D.全部不正确。 |
下列物质中既能使溴水又能使酸性KMnO4溶液褪色的是( )
| A.甲苯 | B.乙烯 | C.苯 | D.己烷 |
乙烯是重要的工业原料,下列有关乙烯叙述正确的是
| A.常温常压下是气体 | B.常温常压下是液体 |
| C.不能使酸性高锰酸钾溶液褪色 | D.在一定条件下能够聚合生成聚乙烯 |
保护环境是每一个公民的责任,下列做法不利于保护环境的是
A.开展煤的综合利用 B.开发和利用太阳能 C推广使用无氟冰箱 D.用火力发电代替风力发电
如右图所示的铜锌原电池中,铜电极为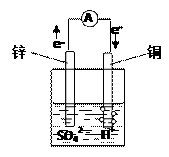
| A.负极 | B.正极 |
| C.发生还原反应的一极 | |
| D.发生氧化反应的一极 |