某酸性溶液中只含NH4+、C1-、H+、OH-四种离子,下列说法正确的是
| A.溶液中离子浓度可能满足:c(C1-)>c(H+)>c(NH4+)>c(OH-) |
| B.该溶液不能由等物质的量浓度、等体积的盐酸和氨水混合而成 |
| C.可由pH=3的盐酸与pH=11的氨水等体积混合而成 |
| D.再通入适量氨气,溶液中离子浓度可能为:c(NH4+)>c(C1-)>c(H+)>c(OH-) |
下列电离或离子方程式正确的是
| A.碳酸的电离方程为:H2CO3⇌2H++CO32- |
| B.NaHS水解方程式为:HS-+H2O⇌H3O++S2- |
| C.用醋酸除去水垢中的氢氧化镁:Mg(OH)2+2CH3COOH=Mg 2+++2CH3COO-+2H2O |
| D.将少量SO2气体通入氨水中:SO2 + NH3·H2O=NH4++ HSO3- |
用NA表示阿伏加德罗常数的数值,下列说法正确的是
| A.0.1mol甲烷中所含的共价键数均为0.4NA |
| B.2.24LN2中含有原子数为0.2NA |
| C.1L 1mol/L的氯化铁溶液中,若Cl—的数目为3NA,则Fe3+的数目为NA |
| D.0.1 molN2和0.3molH2在一定条件下充分反应,转移电子数目为0.6NA |
下列实验装置与描述正确的是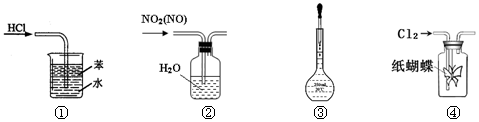
| A.装置①:用于吸收HCl气体 |
| B.装置②:用于除去NO2中的NO |
| C.装置③:配制1mol/L NaCl溶液定容操作 |
| D.装置④:滴有淀粉碘化钾溶液的纸蝴蝶变蓝 |
下列有关物质应用的说法中,正确的是
| A.氢氧化铝具有弱碱性,可用于制胃酸中和剂 |
| B.用二氧化硫加工银耳,使之更白 |
| C.二氧化锰具有强氧化性,故能将双氧水氧化为氧气 |
| D.NH3极易溶于水,可用作制冷剂 |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.使甲基橙变红色的溶液中:NO3-、CO32-、NH4+、Na+ |
| B.使酚酞变红色的溶液中:HCO3-、NO3-、Ba2+、K+ |
| C.0.1mol/LCaCl2的溶液中:HCO3-、NO3-、Na+、K+ |
| D.0.1mol/LFeCl3的溶液中:Mg2+、Na+、Cl-、SCN- |