下列有关氧化还原反应的说法正确的是
| A.阳离子只有氧化性,阴离子只有还原性 |
| B.失电子难的原子获得电子的能力一定强 |
| C.氧化还原反应中的反应物,不是氧化剂就是还原剂 |
| D.非金属元素最高价氧化物的水化物并不一定都具有强氧化性 |
提出元素周期律并根据元素周期律编制第一个元素周期表的科学家是
| A.道尔顿 | B.普利斯特里 | C.门捷列夫 |
D.阿伏加德罗 |
下列烧杯中盛放的都是稀硫酸,在铜电极上能产生大量气泡的是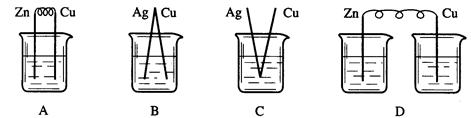
1999年,世界重大科技成果之一是超铀元素的发现,它有力地支持了“稳定岛”假说,原子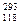 X的中子数为
X的中子数为
| A.0 | B.57 | C.118 | D.175 |
下列叙述正确的是
A.浓硝酸、浓硫酸均能将木炭氧化成二氧化碳
B.Na2O2与水反应,红热的Fe与水蒸气反应 均能生成碱
均能生成碱
C. Li、C、S分别在足量氧气中燃烧均生成一种相应氧化物
D.NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体
下列离子方程式正确的是
A.少量SO2通入 溶液中: 溶液中: |
| B.足量氯气通入溴化亚铁溶液中:3Cl2 + 2Fe2+ + 4Br-="==" 6Cl-+ 2Fe3+ + 2 Br2 |
C.在稀氨水中通入过量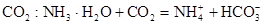 |
| D.澄清石灰水与盐酸反应:Ca(OH)2 + 2 H+ ="==" Ca2+ + 2 H2O |