把铝粉和某铁氧化物xFeO·yFe2O3粉末配成铝热剂,再分成两等份。一份在高温下恰好完全反应后,再与足量盐酸反应;另一份直接放入足量的烧碱溶液中充分反应。前后两种情况下生成的气体质量比是8:11,则x:y为
| A.5:7 | B.7:5 | C.1:2 | D.2:3 |
下列各组原子中,彼此化学性质一定相似的是( )
| A.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子 |
| B.原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子 |
| C.2p轨道上只有一个电子的X原子与3p轨道上只有一个电子的Y原子 |
| D.最外层都只有一个电子的X、Y原子 |
下列电子排布图中,能正确表示该元素原子的最低能量状态的是( )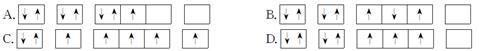
X和Y是原子序数大于4的短周期元素,Xm+和Yn-两种离子的核外电子排布相同,下列说法中正确的是( )
| A.X的原子半径比Y小 | B.X和Y的核电荷数之差为m-n |
| C.电负性X>Y | D.第一电离能X<Y |
某同学在学习核外电子排布的知识时,把15P原子的电子排布式写成了1s22s22P63s23P 3P
3P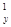 ,他违背了( )
,他违背了( )
| A.能量守恒原理 | B.泡利不相容原理 | C.能量最低原则 | D.洪特规则 |
下列电子排布式中,原子处于激发态的是()
| A.1s22s22P6 | B.1s22s22P33s1 |
| C.1s22s22P63s2 | D.1s22s22P63s23P6 |