碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是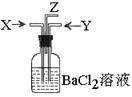
| A.集气瓶中产生的沉淀是硫酸钡 |
| B.Z导管出来的气体中无二氧化碳 |
| C.集气瓶中产生的沉淀是碳酸钡 |
| D.Z导管口有出现气体无色 |
生产、生活离不开各种化学物质,下列说法不正确的是
| A.氧化铝可以用来制造耐火坩埚、耐火管和耐高温的实验仪器 |
| B.潜水艇在紧急情况下可用过氧化钠供氧 |
| C.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 |
| D.工业上常用硅制造光导纤维 |
下列叙述中不正确的是
| A.可用装置①鉴别碳酸钠和碳酸氢钠 | B.可用装置②分离汽油和水的混合物 |
| C.可用装置③将海水蒸馏得到淡水 | D.可用装置④把胶体粒子从分散系中分离出来 |
下列说法正确的是
| A.因海水中含有镁元素,故不需经过化学变化就可以得到金属镁 |
| B.从海水中可得到NaCl,电解熔融NaCl或其水溶液都可制得钠 |
| C.乙烯、丙烯、甲烷等主要化工基本原料都可以由石油分馏得到 |
| D.煤的干馏是化学变化,石油的分馏是物理变化 |
如下图,在25℃,101.3KPa下,将10mLO2全部压入左端盛有20mLNO的注射器中充分反应。
以下对压入O2后左端注射器中的气体描述错误的是
| A.气体变为红棕色 |
| B.气体体积仍为20mL |
| C.气体变为混合物 |
| D.气体中氮原子与氧原子物质的量之比等于l:2 |
某氯化镁溶液的密度为d g/cm3,其中镁离子的质量分数为w,a mL该溶液中Cl—的物质的量为:
| A.mol | B.mol | C.mol | D.mol |