下列离子方程式正确的是
| A.在硫酸氢钾溶液中加入氢氧化钡溶液至pH=7 :Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B.将少量SO2气体通入NaClO溶液中 :SO2+2ClO-+H2O=SO32-+2HClO |
| C.向碳酸氢钠溶液中滴入过量石灰水:HCO3- + Ca2+ + OH-=CaCO3↓+ H2O |
| D.向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:2Al3++ 3SO42-+ 3Ba2+ + 6OH-=2Al(OH)3↓+ 3BaSO4↓ |
利用点滴板探究氨气的性质(如右图所示)。实验时向NaOH 固体上滴几滴浓氨水后,立即用表面皿扣住点滴板。下列对实验现象的解释正确的是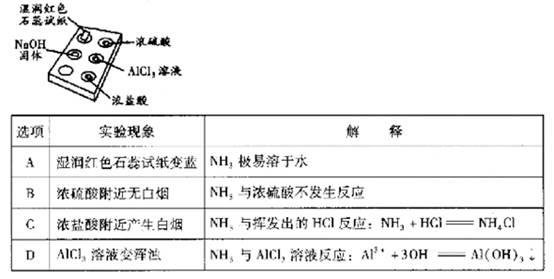
肼(N2H2 )是火箭常用的高能燃料,常温下为液体,其球棍模型如下图所示。肼能与双氧水发生反应: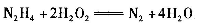 。用NA表示阿伏伽德罗常数,下列说法正确的是
。用NA表示阿伏伽德罗常数,下列说法正确的是
| A.标准状况下,11.2LN2 中含电子总数为5 NA |
| B.标准状况下,22.4LN2 H4中所含原子总数为6 NA |
| C.标准状况下, 3.2gN 2H4中含有共价键的总数为0.6 NA |
| D.若生成3.6gH2 O,则上述反应转移电子的数目为0.2 NA |
右图是元素周期表的一部分,下列关系判断正确的是
| A.原子半径:Y > X > W |
| B.氢化物的沸点:W > X > Y |
| C.氢化物的稳定性:R > Y > X |
| D.简单阴离子的还原性:Y > R > Z |
下列事实与元素周期律相关知识无关的是
| A.向淀粉KI 溶液中滴入溴水,溶液变蓝 |
| B.NaOH 、Mg(OH)2、Al(OH) 3的碱性依次减弱 |
| C.金属钠燃烧呈现黄色火焰,金属钾燃烧呈现紫色火焰 |
| D.F2和H2暗处化合爆炸,而Cl2和H2化合需光照或点燃 |
下列解释事实的方程式不正确的是
A.将NO2通入水中,红棕色消失: |
B.向含有Hg2+的废水中加入Na2S 产生沉淀: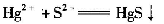 |
C.Na 与水反应产生气体: |
D.向燃煤中加入石灰石可减少SO2 的排放: |