ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含ⅥA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)氧元素能形成繁多的氧化物,请写出一个与CO2等电子的化合物 。
(2)把Na2O、 SiO2、P2O5三种氧化物按熔沸点由高到低顺序排列 。
(3)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,O、S、Se原子的第一电离能由大到小的顺序为 ;
(4)Se原子基态核外电子的排布式为 ;H2Se的沸点:-41.1℃,H2S的沸点:-60.4℃引起两者沸点差异的主要原因是 ;
(5)SO32-离子中硫原子的杂化方式 ,该离子的立体构型为 ;
(6)某金属元素A的氧化物用作玻璃、瓷器的颜料、脱硫剂。其立方晶体的晶胞结构如右图所示,则该氧化物的化学式为 。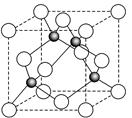
(10)(1)可正确表示原子轨道的是:①。
A.2s B.2d C.3pz D.3f
(2)写出原子序数31的基态镓(Ga)原子的电子排布式:②。
(3)下列物质变化,只与范德华力有关的是③。
A.干冰熔化 B.乙酸汽化
C.乙醇与丙酮混溶 D.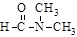 溶于水
溶于水
E.碘溶于四氯化碳 F.石英熔融
(4)下列物质中,只含有极性键的分子是④,既含离子键又含共价键的化合物是⑤,
只存在σ键的分子是⑥,同时存在σ键和π键的分子是⑦。
A.N2 B.CO2 C.CH2Cl2 D.C2H4 E.C2H6 F.CaCl2 G.NH4Cl
(5)用“>” “< ” “=” 填空:
第一电离能的大小:Mg⑧Al;熔点的高低:KCl⑨MgO。
m、n、x、y四种主族元素在周期表的相对位置如下图所示。已知它们的原子序数总和为46,则: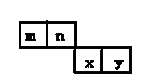
(1)元素n的气态氢化物的分子式为,空间构型为,n原子的价电子排布式是_______
(2)m与y所形成的化合物含键,属分子。(填“极性”或“非极性”)
(3)x位于周期表的第周期第族;其简单离子的离子结构示意图为。
(4)由n、y的氢化物相互作用所生成的物质的电子式为。
(10分)X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种元素为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9。单质Y和W都可与浓的NaOH溶液反应。请回答下列问题:
(1)Y、Z、W的原子半径由小到大的顺序是________。
(2)ZW2的电子式是________。
(3)工业生产单质Y的原理是________________________________________(用化学方程式表示)。
(4)X与Y化学性质相似,则X与浓的NaOH溶液反应的化学方程式是______________________。
(5)0.1 mol的单质W与50 mL 1.5 mol·L-1的FeBr2溶液反应,则被氧化的Fe2+和Br-的物质的量之比是________。
今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行下列实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加足量NaOH溶液加热后,收集到0.04mol气体;
③第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤,干燥后,沉淀质量为2.33g;根据上述实验,推测100mL该溶液中一定存在的离子以及计算这些离子的物质的量。
已知钠能与水剧烈反应:2Na+2H2O=2NaOH+H2↑
(1)相同质量的Na,Mg,Al与过量的盐酸反应,在相同的状况下,三者置换出的H2的体积比是____________________________。
(2)相同物质的量的Na,Mg,Al与过量的盐酸反应,在相同状况下,三者置换出的H2的体积比是_________________________。
(3)Na,Mg,Al与过量的盐酸反应,在相同状况下产生的氢气的体积相等,则Na,Mg,Al三种金属的物质的量之比是__________________________。
(4)将Na,Mg,Al各0.3mol分别投入到含0.1mol HCl的盐酸中,同温同压下产生气体的体积比是_____________________。