Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图,电解总反应为:2Cu+H2O=Cu2O+H2↑。下列说法正确的是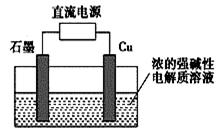
| A.石墨电极上产生氢气 |
| B.铜电极发生还原反应 |
| C.铜电极接直流电源的负极 |
| D.当有0.1 mol 电子转移时,有0.1 mol Cu2O生成 |
某一反应体系中有反应物和生成物共6种:HCl、H2SO4、SnCl2、SnCl4、FeSO4、Fe2(SO4)3,已知反应前在溶液中滴加KSCN溶液呈血红色,反应后红色消失。则该反应中的氧化剂和氧化产物分别是
| A.SnCl4、Fe2(SO4)3 | B.Fe2(SO4)3、SnCl4 |
| C.SnCl2、FeSO4 | D.HCl、H2SO4 |
下列叙述正确的是
| A.发生化学反应时失去电子越多的金属原子,还原性越强 |
| B.金属阳离子被还原后,一定得到该元素的单质 |
| C.核外电子总数相同的原子,一定是同种元素的原子 |
| D.化合反应和置换反应均属于氧化还原反应 |
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系:
甲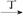 乙
乙 丙。下列有关物质的推断不正确的是
丙。下列有关物质的推断不正确的是
| A.若甲为焦炭,则丁可能是O2 |
| B.若甲为SO2,则丁可能是氨水 |
| C.若甲为Fe,则丁可能是盐酸 |
| D.若甲为NaOH 溶液,则丁可能是CO2 |
下列反应中,不说明SO2是酸性氧化物的是
| A.SO2+H2O===H2SO3 |
| B.SO2+2NaOH===Na2SO3+H2O |
C.2SO2+O2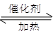 2SO3 2SO3 |
| D.SO2+CaO===CaSO3 |
如果按照某种标准能将FeSO4、Na2SO3、NO划归为同一类物质,则下列物质中也能划归为此类物质的是
| A.KMnO4 | B.Al2(SO4)3 | C.KClO3 | D.K2HPO4 |