向盛有一定量氢氧化钠溶液的烧杯中通入标准状况下448mL氮气和二氧化碳的混合气体后得到溶液A,在溶液A中逐滴加入0.1 mol/L的稀盐酸至过量,并将溶液加热,产生的二氧化碳气体的物质的量与加入稀盐酸的体积的关系如图所示(忽略二氧化碳的溶解和氯化氢的挥发)。下列说法正确的是( )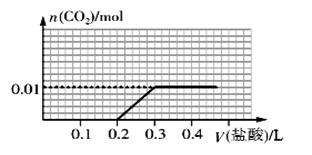
| A.原混合气体中氮气与二氧化碳体积之比为1∶4 |
| B.在逐滴加入稀盐酸产生二氧化碳之前,发生的离子反应为CO32-+H-==HCO3- |
| C.溶 液 A 中 含 有 0 . 01 mol NaOH 和0.01 mol Na2CO3 |
| D.当加入0.1 L稀盐酸时,此时溶液中离子浓度大小关系为c(Na+)>c(Cl-)=c(CO32-)>c(OH-)>c(H+) |