关于下列各装置图的叙述中,不正确的是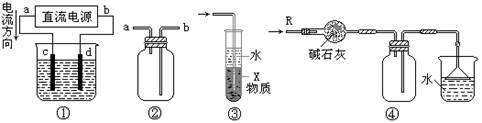
| A.装置①中,d为阳极、c为阴极 |
| B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体 |
| C.装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸 |
| D.装置④可用于干燥、收集氨气,并吸收多余的氨气 |
可逆反应A(s)+B(g) n C (g)△H=Q(n为正整数)在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线如图所示。下列有关叙述中一定正确的是
n C (g)△H=Q(n为正整数)在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线如图所示。下列有关叙述中一定正确的是
| A.其他条件相同, a表示使用了催化剂, b没有使用催化剂 |
| B.其他条件相同,若只改变压强,则a比b的压强大且n≥2 |
| C.其他条件相同,若只改变温度,则a比b的温度高且Q>0 |
| D.其他条件相同,a表示减少A的物质的量 |
已知25℃、101kPa条件下:
4Al (s) + 3O2 (g) = 2Al2O3 (s)△H =-2834.9 kJ/mol
4Al (s) +2O3 (g) = 2Al2O3 (s)△H =-3119.91kJ/mol
由此得出的结论正确的是
| A.等质量的O2比O3能量低,由O2变O3为吸热反应 |
| B.等质量的O2比O3能量低,由O2变O3为放热反应 |
| C.O3比O2稳定,由O2变O3为吸热反应 |
| D.O2比O3稳定,由O2变O3为放热反应 |
已知反应:①101kPa时,C(s) + 1/2O2(g)=CO(g) △H1=-110.5kJ/mol
②稀溶液中,H+(aq) + OH-(aq)=H2O(1) △H2=-57.3kJ/mol
下列结论正确的是()
| A.若碳的燃烧热用△H3来表示,则△H3<△H1 |
| B.若碳的燃烧热用△H3来表示,则△H3>△H1 |
| C.浓硫酸与稀NaOH溶液反应的中和热为57.3kJ/mol |
| D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0 kJ/mol
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);△H=-192.9 kJ/mol
下列说法错误的是
| A.1mol CH3OH(g)完全燃烧放出的热量大于192.9 kJ |
| B.根据反应①和②推知反应: H2(g)+1/2O2(g)=H2O(g)的△H=-241.9kJ/mol |
| C.CH3OH转变成H2的过程不一定要吸收能量 |
| D.反应①中的能量变化如图所示 |
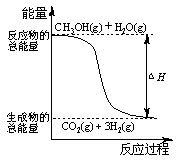
广义的水解观认为,无论是盐的水解还是非盐的水解,其最终结果都是反应中各物质和水分别解离成两部分,然后两两重新组合成新的物质。根据上述观点,下列说法中不正确的是
A.CaO2的水解产物是Ca(OH)2和H2O2 |
B.Al4C3的水解产物是Al(OH)3和甲烷 |
C.PCl3的水解产物是PH3和HClO  |
D.A1(C2H5)3的水解产物是Al(OH)3与C2H6 |