反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g)在10 L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45 mol,则此反应的平均反应速率v(X)(反应物的消耗速率或产物的生成速率)可表示为
4NO(g)+6H2O(g)在10 L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45 mol,则此反应的平均反应速率v(X)(反应物的消耗速率或产物的生成速率)可表示为
| A.v(O2)=0.001 mol·L-1·s-1 | B.v(NH3)=0.01 mol·L-1·s-1 |
| C.v(NO)=0.001 mol·L-1·s-1 | D.v(H2O)=0.045 mol·L-1·s-1 |
绿原酸是咖啡的热水提取液的成分之一,绿原酸结构简式如下: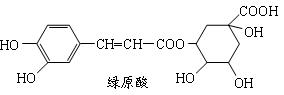
下列关于绿原酸判断不正确的是()
| A.绿原酸既可以催化加氢,又可以使酸性KMnO4溶液褪色 |
| B.绿原酸有一个官能团叫羧基 |
| C.1mol绿原酸与足量NaOH溶液反应,最多消耗2mol NaOH |
| D.绿原酸可以与FeCl3溶液发生显色反应 |
下列有关电化学的示意图中正确的是( )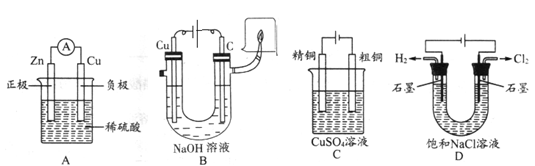
对下列反应改变反应物用量,不能用同一个离子方程式表示的是 ( )[来
①NaHCO3溶液与石灰水反应
②Na2SO3溶液与稀盐酸反应
③Si与烧碱溶液反应
④Fe与稀硝酸反应
| A.①②③ | B.①②④ | C.①③④ | D.②③④ |
下列是某同学对相应反应的离子方程式所作的评价,其中评价合理的是()
| 编号 |
化学反应 |
离子方程式 |
评价 |
| ① |
硫酸溶液中 加入Ba(OH)2溶液 加入Ba(OH)2溶液 |
Ba2++SO=BaSO4↓ |
正确 |
| ② |
氧化铝与NaOH溶液反应 |
2Al3++3O2-+2OH-= 2AlO+H2O |
错误,Al2O3不应写成离子形式 |
| ③ |
铁和稀硝酸反应 |
Fe+2H+===H2↑+Fe2+ |
正确 |
| ④ |
等物质的量的FeBr2和Cl2反应 |
2Fe2++2Br +2Cl2=2Fe3++Br2+4Cl- +2Cl2=2Fe3++Br2+4Cl- |
错误,离子方程式中Fe2+与Br-的物质的量之比与化学式不符 |
| A.只有② | B.①③ | C.②④ | D.①②③④ |
在一瓶无色未知溶液中检验出有Ba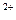 、Ag
、Ag ,同时又测得其酸性很强。某学生还要鉴定此溶液中是否大量存在:①Cu
,同时又测得其酸性很强。某学生还要鉴定此溶液中是否大量存在:①Cu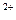 、②Fe
、②Fe 、③ Cl
、③ Cl 、④ NO
、④ NO 、⑤ S
、⑤ S 、⑥ CO
、⑥ CO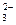 、⑦ NH
、⑦ NH 、⑧ Mg
、⑧ Mg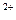 、⑨A1
、⑨A1 、⑩
、⑩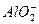 离子。其实,这些离子中有一部分不再鉴定就能加以否定,你认为不必鉴定的离子组是()
离子。其实,这些离子中有一部分不再鉴定就能加以否定,你认为不必鉴定的离子组是()
| A.③⑤⑥⑦⑩ | B.①②⑤⑥⑧⑨ | C.③④⑦⑧⑨ | D.①②③⑤⑥⑩ |