将标准状况下的a L HCl(g)溶于1000 g水中,得到的盐酸密度为b g/cm3,则该盐酸的物质的量浓度是( )
A. mol·L-1 mol·L-1 |
B. mol·L-1 mol·L-1 |
C. mol·L-1 mol·L-1 |
D. mol·L-1 mol·L-1 |
钾长石的主要成分为硅酸盐,由前20号元素中的四种组成,化学式为XYZ3W8,其中只有W显负价。X、Y的最外层电子数之和与Z的最高正价数相等,Y3+与W的阴离子具有相同的电子层结构,X、W的质子数之和等于Y、Z的质子数之和。下列说法错误的是
| A.离子半径:X>Y |
| B.氢化物的稳定性:W>Z |
| C.化合物X2W2和Y2W3中都不含共价键 |
| D.1 mol ZW2晶体所含Z-W键的数目为4NA(NA为阿伏加德罗常数的值) |
下列是某同学对相应的离子方程式所作的评价,其中评价合理的是
| 编号 |
化学反应 |
离子方程式 |
评价 |
| A |
碳酸钙与 醋酸反应 |
CO32-+2CH3COOH=CO2↑+H2O+2CH3COO- |
错误,碳酸钙是弱电解 质,不应写成离子形式 |
| B |
苯酚钠溶液中 通入CO2 |
2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
正确 |
| C |
NaHCO3的水解 |
HCO3-+H2O=CO32-+H3O+ |
错误,水解方程式 误写成电离方程式 |
| D |
等物质的量的FeBr2和Cl2反应 |
2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
错误,离子方程式中 Fe2+与Br-的物质的量 之比与化学式不符 |
某有机物的结构简式如图,下列关于该有机物的叙述正确的是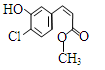
| A.该有机物的摩尔质量为200 |
| B.该有机物属于芳香烃 |
| C.该有机物可发生取代、加成、加聚、氧化、还原、消去反应 |
| D.1 mol该有机物在适当条件下,最多可与4mol NaOH和4mol H2反应 |
下列有关实验原理或实验操作正确的是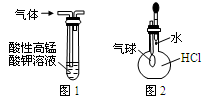
| A.用干燥pH试纸测定某新制氯水的pH |
| B.用图1装置除去乙烷中混有的乙烯 |
| C.用图2装置能验证HCl气体在水中的溶解性 |
| D.用25mL碱式滴定管量取20.00mL KMnO4溶液 |
下列叙述不正确的是
| A.根据某元素原子的质子数和中子数,可以确定该元素的相对原子质量 |
| B.CaCl2、MgCl2晶体都容易潮解,它们潮解的实质是晶体表面吸水形成溶液 |
| C.根据金属活动性顺序表,可以推断冶炼金属时可能的方法 |
| D.根据酸、碱、盐的溶解性表,可以判断某些溶液中的复分解反应能否进行 |