“绿色化学”又称“环境友好化学”,其目的是研究和寻找能充分利用的无毒无污染原材料,最大限度的节约能源,在化工生产中实现净化和无污染。下列各项属于“绿色化学”的是( )
| A.处理废弃物 | B.治理污染点 |
| C.杜绝污染源 | D.减少有毒物 |
已知:①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;②向FeCl2溶液中通入少
量实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。下列判断正确的是( )
| A.上述实验证明还原性:MnO-4>Cl2>Fe3+>I2 |
| B.上述实验中,共有两个氧化还原反应 |
| C.实验①生成的气体能使湿润的淀粉KI试纸变蓝 |
| D.实验②证明Fe2+既有氧化性又有还原性 |
化学与生活、生产有着密切的联系,下列说法正确的是( )
| A.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” |
| B.废弃的塑料、金属、纸制品及玻璃都是可回收再利用的资源 |
| C.凡含有食品添加剂的食物对人体健康均有害,不宜食用 |
| D.钢铁在海水中比在河水中更易腐蚀,主要原因是海水含氧量高于河水 |
在一定温度和压强下,下列各可逆反应达到化学平衡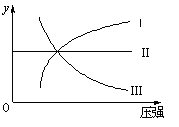
状态,各反应有如图所示的对应关系:
(1)N2(g)+3H2(g) 2NH3(g)△H<0(曲线Ⅰ)
2NH3(g)△H<0(曲线Ⅰ)
(2)H2(g)+I2(g) 2HI(g)△H>0(曲线Ⅱ)
2HI(g)△H>0(曲线Ⅱ)
(3)2SO3(g) 2SO2(g)+O2(g)△H>0(曲线Ⅲ)
2SO2(g)+O2(g)△H>0(曲线Ⅲ)
则图像中y轴可以表示()
①平衡混合气中一种生成物的体积分数②平衡混合气中一种反应物的体积分数③平衡混合气中一种生成物的产率④平衡混合气中一种反应物的转化率
| A.①②③ | B.①②④ | C.①③④ | D.②③④ |
已知某弱酸的酸式盐有NaH2XO4和Na2HXO4,其中NaH2XO4的溶液呈酸性,Na2HXO4溶液呈碱性。30℃时,浓度均为0.1mol•L-1NaH2XO4溶液和Na2HXO4溶液中均存在的关系是()
| A.c(H+)•c(OH-) >1×10-14 |
| B.c(H+) + 2c(H3XO4)+ c(H2XO4-)=c(XO43-)+ c(OH-) |
| C.c(H+) + c(H3XO4)= c(HXO42-)+ 2c(XO43-)+ c(OH-) |
| D.c(Na+)+ c(H+)= c(H2XO4-)+ c(OH-)+ 2c(HXO42-)+ 3c(XO43-) |
2008年北京残奥会吉祥物是以牛为形象
设计的“福牛乐乐”(Funiulele)。有一种有机
物的键线式也酷似牛形(右图所示),故称为
牛式二烯炔醇(cowenyenynol)。
下列有关说法正确的是 ()
| A.该有机物的化学式为:C29H44O |
| B.牛式二烯炔醇含有5个手性碳原子 |
| C.1mol牛式二烯炔醇最多可与6molBr2发生加成反应 |
| D.牛式二烯炔醇分子内能发生消去反应 |