炼铁的还原剂CO是由焦炭和CO2反应而得。现将焦炭和CO2放入体积为2L的密闭容器中,高温下进行下列反应:

 。右图为CO2、CO的物质的量n随时间t的变化关系图。下列说法正确的是( )
。右图为CO2、CO的物质的量n随时间t的变化关系图。下列说法正确的是( )
| A.0~1min,v(CO)=1mol/(L·min);1~3min时, |
B.当溶器内的压强不变时,反应一定达到平衡状态且 |
| C.3min时温度由T1升高到T2,则可以判断Q>0 |
| D.5min时再充入一定量的CO,n(CO)、n(CO2)的变化可分别由a、b曲线表示 |
如图所示,在火棉胶袋(半透膜)内注入淀粉和食盐溶液,用线系紧密封使玻璃管内的液面刚好高出烧杯内蒸馏水的液面,过一段时间后,用碘酒和硝酸银溶液分别检验蒸馏水,整个实验过程中,所观察到的现象是( )
| A.细玻璃管内液面下降 | B.细玻璃管内液面不变 |
| C.蒸馏水遇碘酒变蓝 | D.蒸馏水遇AgON3溶液有白色沉淀生成 |
等物质的量的主族金属A、B、C分别与足量的稀盐酸反应,所得氢气的体积依次为VA、VB、VC(以上体积均为相同条件下测得),已知VA=3VC,且VA=VB+VC,则在B的反应生成物中,该金属元素的化合价为( )
A.+1 B.+2 C.+3 D.+4
有机物分子中原子(或原子团)间的相互影响会导致它们化学性质的改变。下列叙述能说明上述观点的是( )
| A.苯酚能与NaOH溶液反应,而乙醇不能 |
| B.四酸可发生银镜反应,而乙酸不能 |
| C.乙烯可发生加成反应,而乙烷不能 |
| D.等物质的量的甘油和乙醇分别与足量的金属钠反应,甘油产生的H2多 |
已知酸性大小:羧酸>碳酸>酚.下列含溴化合物中的溴原子,在适当条件下都能被羟其(-OH)取代(均可称之为水解反应),所得产物能跟NaHCO3溶液反应的是( )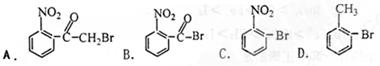
金刚烷的结构如图,它可看作是由四个等同的六元环组成的空间构型。请根据中学学过的异构现象判断由氯原子 取代金刚烷亚甲基(-CH2-)中氢原子所形的二氯取代物的种类( )
取代金刚烷亚甲基(-CH2-)中氢原子所形的二氯取代物的种类( )
| A.4种 | B.3种 |
| C.2种 | D.6种 |