配制100mL1.0mol·L-1的NaOH溶液,下列情况不会影响溶液浓度的是( )
| A.容量瓶使用前有蒸馏水 |
| B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒 |
| C.俯视确定凹液面与刻度线相切 |
| D.称量NaOH固体时使用了称量纸 |
下列说法正确的是
A.pH=5的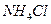 溶液或醋酸中,由水电离出的 溶液或醋酸中,由水电离出的 均为10 均为10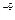 mol/L mol/L |
| B.pH=3的醋酸和pH=11的NaOH溶液等体积混合后,pH>7 |
C.在c(H ):c(OH ):c(OH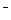 )=1:10 )=1:10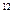 的溶液中,Na 的溶液中,Na 、I 、I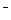 、 、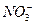 、 、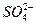 能大量共存 能大量共存 |
D.0.1 mol/L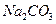 溶液和0. 1 mol/L 溶液和0. 1 mol/L 溶液等体积混合,溶液中 溶液等体积混合,溶液中 |

下列说法正确的是
A.将铁粉加入 、 、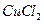 混合溶液中,充分反应后剩余的固体中必有铁 混合溶液中,充分反应后剩余的固体中必有铁 |
B.将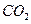 和 和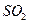 混合气体分别通入 混合气体分别通入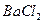 溶液、 溶液、 溶液中,最终都有沉淀生成 溶液中,最终都有沉淀生成 |
C.检验某酸性溶液中 和 和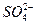 ,选用试剂及顺序是过量 ,选用试剂及顺序是过量 溶液、 溶液、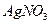 溶液 溶液 |
D.用加热分解的方法可将 固体和Ca(OH)2固体的混合物分离 固体和Ca(OH)2固体的混合物分离 |
4种短周期元素W、X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为19,W和X元素原子内质子数之比为1:2,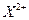 和
和 离子的电子数之差为8。下列说法不正确的是
离子的电子数之差为8。下列说法不正确的是
| A.与W相邻的同主族元素可制成重要的半导体材料 |
| B.元素原子半径从大到小的顺序是X、Y、Z |
| C.WZ4分子中W、Z原子通过共价键结合且最外层均达到8电子结构 |
D.W、Y、Z元素最高价氧化物对应的水化物中酸性最强的是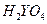 |
下列实验操作不能达到其对应目的的是
| 编号 |
实验操作 |
目的 |
| A |
取 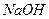 加入96mL水中 加入96mL水中(水的密度近似看作1g/ 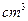 ) ) |
配置4%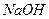 溶液 溶液 |
| B |
滴定实验中,用待测液润洗锥形瓶 |
避免造成误差使滴定结果偏低 |
| C |
向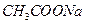 溶液中滴入酚酞溶液,加热 溶液中滴入酚酞溶液,加热 |
证明升高温度能促进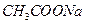 水解 水解 |
| D |
向盛有铜片的试管中加入浓硫酸,加热 |
证明浓硫酸具有强氧化性 |
反应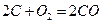 的能量变化如右图所示。下列说法正确的是
的能量变化如右图所示。下列说法正确的是
A.12 g C(s)与一定量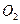 (g)反应生成14 g CO(g),放出的热量为110.5 kJ (g)反应生成14 g CO(g),放出的热量为110.5 kJ |
B.2 mol C(s)与足量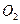 (g)反应生成 (g)反应生成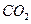 (g),放出的热量大于221 kJ (g),放出的热量大于221 kJ |
C.该反应的热化学方程式是 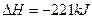 |
D.该反应的反应热等于CO分子中化学键形成时所释放的总能量与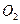 分子中化学键断裂时所吸收的总能量的差 分子中化学键断裂时所吸收的总能量的差 |