蔗糖和麦芽糖的分子式均为C12H22O11,但在一定条件下,一分子蔗糖水解(即和水反应)生成一分子葡萄糖(C6H12O6)和一分子果糖(C6H12O6),一分子麦芽糖水解生成两分子葡萄糖。葡萄糖和果糖虽然分子是相同,但结构不同。由此可知,蔗糖和麦芽糖互为 。
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。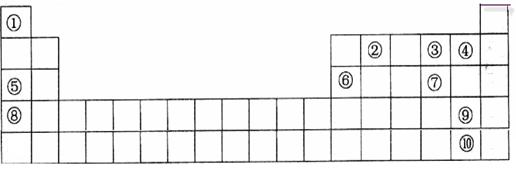
用化学符号回答下列问题:
(1)表中最活泼的金属与最活泼的非金属形成的物质是;
(2)⑤、⑥、⑧的最高价水化物的碱性由强到弱的顺序是;
③、④、⑦氢化物稳定性由强到弱的顺序是;
(3)③与⑤按原子个数1:1所成的化合物的电子式为________________;该化合物与水反应的离子方程式为________________。
(4)⑥号元素最高氧化物水化物与⑤号元素最高价氧化物水化物反应的离子方程式为;
(5)请设计一个实验方案,比较⑨、⑩的单质氧化性的强弱:。
下列五种物质中① Ar② H2O2③ NH4 NO3④ KOH⑤ Na2O2⑥ CaCl2只存在共价键的是,只存在离子键的是,既存在共价键又存在离子键的是,不存在化学键的是。(填写序号)
(10分)今有化合物:
(1)请写出丙中含氧官能团的名称:;
(2)请判别上述哪些化合物互为同分异构体:;
(3)请分别写出鉴别甲、乙、丙化合物的方法。(指明所选试剂及主要现象即可)
鉴别甲的试剂:;现象:;
鉴别乙的试剂:;现象:;
鉴别丙的试剂:;现象:;
下图是维生素A的分子结构:
(1)维生素A中的含氧官能团是(写名称);
(2)维生素A的分子式是;
(3)通常情况下1mol维生素A最多能与mol溴反应;
(4)试指出维生素A可能发生的化学反应类型(任写一种即可)。
下图表示某淡黄色固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。B和C的相对分子质量相差16,化合物D是重要的工业原料。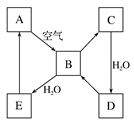
(1)单质A的名称 ________。
(2)写出E与A的氢化物反应生成A的化学方程式__________________________。
(3)写出一个由D生成B的化学方程式______________________。