某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动。
【提出问题】这种淡黄色粉末是什么?有什么性质和用途?
【查阅资料】①硫是淡黄色粉末,不溶于水;②过氧化钠(Na2O2)是淡黄色粉末,在常温下能与水反应生成碱和一种气体;在呼吸面具中和潜水艇里常用作供氧剂。
【猜想与探究】猜想:淡黄色粉末可能是:a.硫;b.过氧化钠;c.硫和过氧化钠的混合物。
探究:过氧化钠与水反应的生成物的成分。
【实验与结论】
| |
实验操作 |
实验现象 |
实验结论 |
| 猜想 |
在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水 |
_____________________ |
猜想a、c不成立,猜想b成立。 |
| 探究 |
①用带火星的木条伸入过氧化钠与水反应的试管中 |
木条复燃 |
生成物有___________ |
| ②往①试管内的溶液中滴加___________ ______________ |
_____________________ |
生成物有氢氧化钠 |
【继续探究】小组对过氧化钠能作为供氧剂也很感兴趣,大家讨论认为可能是CO2在常温下能与过氧化钠反应有关,
于是设计上图所示的装置继续实验探究。
| 实验操作 |
实验现象 |
实验结论 |
| ①将CO2从a口处通入装置内,再把带火星的木条放在装置b口处 |
木条复燃 |
CO2在常温下能与过氧化钠反应,该反应的化学方程式为: ____________________________ |
| ②取出充分反应后的固体生成物于试管中,往试管内滴加稀盐酸,将生成的氢气通入澄清石灰水中 |
有气泡产生 石灰水变浑浊 |
【交流与比较】与我们学过的制氧气方法相比,常选用过氧化钠作为呼吸面具和潜水艇的供氧剂的一个理由是: ________________________________。
在实验室模拟工业生产碳酸钠:一定温度下,往一定量饱和NaCl溶液中通入氨气达到饱和后,再不断通入CO2,一段时间后,出现沉淀,过滤得到NaHCO3晶体。
(1)该过程的化学方程式:。
(2)加热NaHCO3得到纯碱制品,实验室可进行此操作的装置是。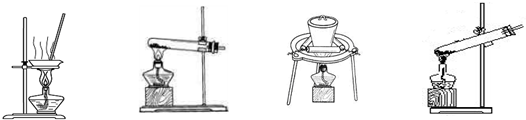
A B C D
(3)得到的纯碱制品含有少量NaHCO3和NaCl,设计实验验证样品中各种组分。试剂和仪器限选用:试管、胶头滴管、过滤装置、Ba(NO3)2溶液、NaOH溶液、AgNO3溶液、澄清石灰水、稀硫酸、稀盐酸、稀硝酸。
| 步骤一:取少量制品于试管中,加少量蒸馏水,振荡,溶解。往试管中加入 振荡,观察 |
现象:溶液中产生大量白色沉淀; 结论:。 |
| 步骤二:将步骤一的浊液过滤,取滤液于试管中B中,加入, 振荡,观察 |
现象:; 结论:样品中含有NaHCO3。 |
| 步骤三:将步骤二的浊液过滤,取滤液于试管C中, 振荡,观察 |
现象:; 结论:。 |
(4)用碘量法测量自来水中残留的Cl2的浓度:
① 在大锥形瓶中放置过量的KI,加一定量的冰醋酸,准确取水样200mL加入瓶中,迅速塞上瓶塞摇动,水样呈淡黄色,发生反应:Cl2+2I-=2Cl-+ I2。
②加少许淀粉溶液,用cmol/L Na2S2O3溶液滴定,发生反应:I2+2S2O32-=2I-+S4O62-,当,达到滴定终点。
③重复操作3次,平均读数为V mL,则该样品中残留Cl2的浓度:mg/L(Cl的相对原子质量:35.5)
钡盐生产中排出大量的钡泥[主要含BaCO3、BaSO3、Ba(FeO2)2等],某主要生产BaCO3的化工厂利用钡泥制取Ba(NO3)2晶体及其他副产物,其部分工艺流程如下: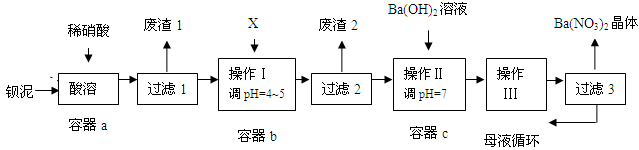
已知:① Fe(OH)3和Fe(OH)2完全沉淀时,溶液的pH分别为3.2和9.7
② Ba(NO3)2在热水中溶解度较大,在冷水中溶解度较小
③ KSP(BaSO4)=1.1×10-10,KSP (BaCO3)=5.1×10-9
(1)该厂生产的BaCO3因含有少量BaSO4而不纯,提纯的方法是:将产品加入足量的饱和Na2CO3溶液中,充分搅拌,过滤,洗涤。用离子方程式说明提纯原理:。
(2)上述流程酸溶时,Ba(FeO2)2与HNO3反应生成两种硝酸盐,化学方程式为:
。
(3)该厂结合本厂实际,选用的X为;
| A.BaCl2 | B.BaCO3 | C.Ba(NO3)2 | D.Ba(OH)2 |
(4)废渣2为。
(5)操作III为。
(6)过滤3后的母液应循环到容器中。(填“a”、“b”或“c”)
(7)称取w克晶体溶于蒸馏水,加入足量的硫酸,充分反应后,过滤、洗涤、干燥,称量沉淀质量为m克,则该Ba(NO3)2的纯度为(相对分子质量:Ba(NO3)2为261,BaSO4为233)。
乙酰水杨酸俗称阿司匹林,是一种历史悠久的解热镇痛药。合成原理是: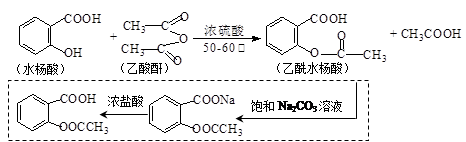
虚框中为提纯原理,是为了除去该反应的副产物:水杨酸酐、乙酰水杨酸水杨酯、乙酰水杨酸酐和聚合物等。水杨酸(熔点158℃)和乙酰水杨酸(熔点135℃)微溶于冷水、可溶于热水和乙酸乙酯。生产流程是: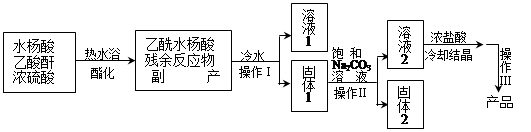
(1)操作I、III的名称是;使用热水浴加热的原因是。
(2)可以循环利用的是;固体2的成份是。
(3)为了检验产品中是否含有水杨酸,并进行精制(除去产品中的其它反应物和副产物),进行以下操作,请完成下表:
| 序号 |
操作 |
现象 |
结论 |
| 检 验 |
取几粒产品晶体投入装适量热水的试管中,振荡 |
得无色溶液 |
|
| 向试管中滴入溶液 |
. |
产品中有水杨酸 |
|
| 重 结晶 |
将粗产品溶于适量的水中,水浴加热,趁热过滤,将滤液,抽滤 |
有晶体析出 |
精产品 |
(4)用中和法测定产品纯度:
取a g产品溶解于V1 mL1mol/L的NaOH溶液中,加热使乙酰水杨酸水解,再用1 mol/L的盐酸滴定过量的NaOH,当滴定终点时消耗盐酸V2 mL;计算出产品纯度为(只需列出计算表达式,不必化简。乙酰水杨酸分子量为180)。
铁触媒(铁的氧化物)是硫酸工业的催化剂。某同学设计了以下两种方案研究铁触媒的组成。
方案一:用下列装置测定铁触媒的含铁量,确定其组成。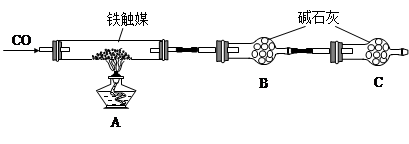
方案二:用下列实验方法测定铁触媒的含铁量,确定其组成。
(1)步骤④中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和 。
(2)因为通入Cl2不足量,“溶液B”中还含有会影响测定结果。
(3)因为通入Cl2过量且加热煮沸不充分,“溶液B”中可能含有Cl2。请设计实验方案检验Cl2,完成下列实验报告。
限选试剂:0.1mol·L-1酸性KMnO4溶液、紫色石蕊试液、品红稀溶液、淀粉-KI溶液、0.1moL·L-1KSCN溶液
| 实验操作 |
实验现象与结论 |
(4)“干燥管C”的作用是。
(5)称取15.2g铁触媒进行上述实验。充分反应后,测得“干燥管B”增重11.0g,则该铁触媒的化学式可表示为。
钒及化合物用途广泛。工业上常用含少量Al2O3的钒铁矿(FeO×V2O5)碱熔法提取V2O5。简要工艺流程如下:
已知:①焙烧时可发生反应:V2O5+Al2O3+2Na2CO3 2NaVO3+2NaAlO2+2CO2↑
2NaVO3+2NaAlO2+2CO2↑
②常温下物质的溶解度:NaVO3~21.2 g /100g水;HVO3~0.008 g/100g水
(1)“浸出渣B”的主要成分是。(写化学式)
(2)生产中,不直接用H2SO4浸泡“烧渣A”获取HVO3的原因是。
(3)“操作①”包括、洗涤。如果不洗涤,则产品中可能含有的金属阳离子是、。下列装置(部分夹持仪器省去)可用在实验室进行“操作②”的是。(填序号)
A B C D
(4)NaVO3用于原油的脱硫技术,由V2O5溶于NaOH溶液中制取,反应的离子方程式为。
(5)V2O5还可用于将硅铁炼成钒铁。生产中加入CaO可节能减排。有关反应如下:
2V2O5(l)+ 5Si(s)+ 5CaO(s)=" 4V(s)+" 5CaSiO3(s)△H1 =" —2096.7" kJ/mol
已知:CaSiO3(s)=" CaO(s)+" SiO2(s)△H2 =" +92.5" kJ/mol
则:2V2O5(l)+ 5Si(s)=" 4V(s)+" 5SiO2(s)△H3 = 。