普通黄铜仅由铜和锌组成,广泛用于制造板材、管材等,也用于铸造机械零件。为测定黄铜中铜的质量分数,取样品10 g,分四次向其中加入稀硫酸使之充分反应,实验数据记录如下表:
| |
第一次 |
第二次 |
第三次 |
第四次 |
| 加入稀硫酸的质量/g |
10 |
10 |
10 |
10 |
| 剩余固体的质量/g |
8.7 |
7.4 |
7 |
7 |
认真分析数据,回答下列问题:
(1)该过程中发生反应的化学方程式为 。
(2)黄铜中铜的质量分数为 。
(3)加入的稀硫酸溶液中硫酸的质量分数是 。(写出计算过程)
某小组利用实验数据,求算金属M的相对原子质量。已知金属M和硫酸反应的化学方程式为: M + H2SO4 ="=" MSO4 + H2↑。
现取20 g该金属样品于烧杯中,然后向其中加入稀硫酸,实验数据记录如下:
| 实验编号 |
1 |
2 |
3 |
4 |
5 |
| 加入硫酸的质量/g |
100 |
200 |
300 |
400 |
500 |
| 烧杯中剩余物质量/g |
119.8 |
219.6 |
319.4 |
419.4 |
519.4 |
第5次实验后,烧杯中还有0.5 g剩余固体。计算该金属的相对原子质量。
氮化铝(AlN)是一种新型材料,是良好的耐热材料,还被大量应用于微电子学。将高纯度铝粉放在氮气流中,在820℃左右反应,可以制得氮化铝。反应的化学方程式是2Al +N2 2AlN。若有54 kg高纯度铝粉,求可制得氮化铝的质量。
2AlN。若有54 kg高纯度铝粉,求可制得氮化铝的质量。
小刚想用贝壳(主要成分为碳酸钙)制取二氧化碳气体。为测定贝壳中碳酸钙的含量,他做了如下实验:首先称取50g贝壳样品于烧杯中,烧杯质量为100克。然后将150g的盐酸平均分5次加入(假设杂质均不溶于水也不与盐酸反应)到烧杯中。实验过程中的数据记录如下:
| 实验次数 |
第一次 |
第二次 |
第三次 |
第四次 |
第五次 |
| 烧杯+剩余物质质量 |
175.6g |
X |
226.8g |
252.4g |
280.2g |
(1)X=g;
(2)贝壳样品中碳酸钙的质量分数;
(3)第三次实验后所得溶液中溶质的质量分数。
工业上常用电解饱和食盐水的方法制备氢氧化钠,其化学方程式为:
2NaCl+2H2O 2NaOH+Cl2↑+H2↑。若制得40g氢氧化钠,同时可得到氢气的质量是多少?
2NaOH+Cl2↑+H2↑。若制得40g氢氧化钠,同时可得到氢气的质量是多少?
为了测定某纯碱样品中碳酸钠和氯化钠的含量(其他成分可忽略),将一定量的该样品溶解在100g水中,加入足量的氯化钙溶液,反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl,反应中物质间的质量关系如右图所示。当反应恰好完成时过滤,测得滤液中氯化钠的质量分数为6%。试计算该样品中: 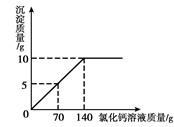
(1)氯化钠的质量;
(2)碳酸钠的质量分数。