工业、农业及城市污水中含有磷,家用洗涤剂是污水中磷的一个重要来源(洗涤剂中含有三聚磷酸钠)。下列关于污水处理时除磷的说法中,正确的是 ( )
| A.磷是生物的营养元素,不必除去 |
| B.含磷的污水是很好的肥料,不必除去 |
| C.含磷的污水排放到自然界中引起藻类过度繁殖,使水变质,需要除去 |
| D.磷对人无害,除去与否都无关紧要 |
下列物质的工业制备原理的方程式书写正确的是
A.乙醇:C6H12O6 2CH3CH2OH+2CO2↑ 2CH3CH2OH+2CO2↑ |
B.乙烯:CH3CH2OH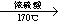 CH2=CH2↑+ H2O CH2=CH2↑+ H2O |
C.盐酸:NaCl+H2SO4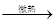 NaHSO4+HCl↑ NaHSO4+HCl↑ |
| D.纯碱:2NaCl+2NH3+CO2+H2O → Na2CO3↓+ 2NH4Cl |
25℃ 时纯水的电离度α1,PH=11的氨水中水的电离度为α2,pH=3的盐酸中水的电离度α3.若将上述氨水与盐酸等体积混合,所得溶液中的电离度为α4下列关系式中正确的是
| A.α1<α2<α3<α4 | B.α3=α2<α1<α4 |
| C.α2<α3<α1<α4 | D.α2=α3<α4<α1 |
碘在不同状态下(固态或气态)与氢气反应的热化学方程式如下所示:
① H2(g)+I2(?) 2HI(g)+9.48kJ② H2(g)+I2(?)
2HI(g)+9.48kJ② H2(g)+I2(?) 2HI(g)-26.48kJ
2HI(g)-26.48kJ
下列判断正确的是
| A.①中的I2为固态,②中的I2为气态 |
| B.②的反应物总能量比①的反应物总能量低 |
| C.①的产物比反应②的产物热稳定性更好 |
| D.1mol 固态碘升华时将吸热17kJ |
某可逆反应aA+bB cC+Q在某温度下的平衡常数为K(K≠1),反应热为Q。保持温度不变,将方程式的书写作如下改变,则Q和K数值的相应变化为
cC+Q在某温度下的平衡常数为K(K≠1),反应热为Q。保持温度不变,将方程式的书写作如下改变,则Q和K数值的相应变化为
A.写成2aA+2bB 2cC,Q值、K值均扩大了一倍 2cC,Q值、K值均扩大了一倍 |
B.写成2aA+2bB 2cC,Q值扩大了一倍,K值保持不变 2cC,Q值扩大了一倍,K值保持不变 |
C.写成cC aA+bB,Q值、K值变为原来的相反数 aA+bB,Q值、K值变为原来的相反数 |
D.写成cC aA+bB,Q值变为原来的相反数,K值变为倒数 aA+bB,Q值变为原来的相反数,K值变为倒数 |
下列变化中,可逆性最不明显的是
| A.NH3+H2O→NH3·H2O | B.Br2+H2→2HBr |
| C.H2+I2→2HI | D.HClO→H++ClO- |