镍镉可充电电池在现代生活中有广泛应用,它的充、放电反应按下式进行:
Cd+2NiOOH+2H2O 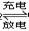 Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
由此可知,该电池放电时的负极是 ( )
| A.Cd | B.NiOOH | C.Cd(OH)2 | D.Ni(OH)2 |
9.2 g金属钠投入到足量的重水中,则产生的气体中含有( )
| A.0.2 mol中子 | B.0.4 mol电子 | C.0.2 mol质子 | D.0.4 mol分子 |
将0.4 g NaOH和1.06 g Na2CO3混合并配成溶液,向溶液中滴加0.1 mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2物质的量的关系是( )
某溶液中阳离子只含K+,其中Cl-、Br-、I-的个数比为1∶2∶3,欲使这些离子个数比变为3∶2∶1,需要通入的氯分子与原溶液中I-的个数比应为( )
| A.1∶2 | B.2∶1 | C.1∶3 | D.3∶1 |
把0.05 mol NaOH固体分别加入到100 mL下列液体中,溶液的导电能力变化最小的是( )
| A.自来水 | B.0.5 mol·L-1盐酸 | C.0.5 mol·L-1CH3COOH溶液 | D.0.5 mol·L-1 KCl溶液 |
氧化还原反应与四种基本反应类型的关系如下图所示,则下列化学反应属于丙区域的是( )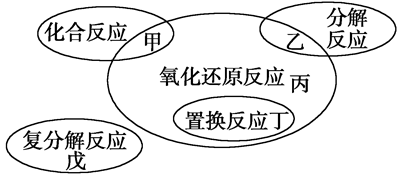
| A.Cl2+2KBr=Br2+2KCl | B.2NaHCO3 Na2CO3+H2O+CO2↑ Na2CO3+H2O+CO2↑ |
C.3Mg+N2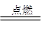 Mg3N2 Mg3N2 |
D.2Na2O2+2CO2=2Na2CO3+O2 |