已知反应 是可逆反应。设计如图装置(
是可逆反应。设计如图装置( 、
、 均为石墨电极),分别进行下述操作。
均为石墨电极),分别进行下述操作。
Ⅰ.向B烧杯中逐滴加入浓盐酸
Ⅱ.向B烧杯中逐滴加入40% NaOH溶液
结果发现电流计指针均发生偏转.据此,下列判断正确的是
| A.操作Ⅰ过程中,C1为正极 |
| B.操作Ⅱ过程中,盐桥中的K+移向B烧杯溶液 |
| C.Ⅰ操作过程中,C2棒上发生的反应为:AsO43-+2H++2e-=AsO33-+H2O |
| D.Ⅱ操作过程中,C1棒上发生的反应为:2I――2e-=I2 |
下表是三种难溶金属硫化物的溶度积常数(25℃):
| 化学式 |
FeS |
CuS |
MnS |
| 溶度积 |
6.3×10-18 |
1.3×10-36 |
2.5×10-13 |
下列有关说法中正确的是()
A.25℃时,CuS的溶解度大于MnS的溶解度
B.25℃时,饱和CuS溶液中,Cu2+的浓度为1.3×10-36 mol•L-1
C.因为H2SO4是强酸,所以反应CuSO4+H2S=CuS↓+H2SO4不能发生
D.除去某溶液中的Cu2+,可以选用FeS作沉淀剂
对于可逆反应:2A(g)+B(g) 2C(g)△H<0。下列与该反应相关的各图中,正确的是
2C(g)△H<0。下列与该反应相关的各图中,正确的是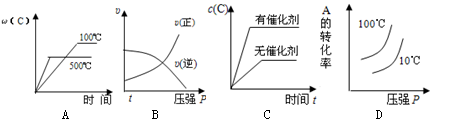
低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:发生的化学反应为:
2NH3(g)+NO(g)+NO2(g)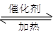 2N2(g)+3H2O(g)△H<0
2N2(g)+3H2O(g)△H<0
在恒容的密闭容器中,下列有关说法正确的是()
| A.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
| B.平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小 |
| C.其他条件不变,充入惰性气体,正逆反应速率均不发生变化,平衡不移动 |
| D.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 |
某化学反应中,反应混合物A、B、C的物质的量浓度(c)与时间(t)关系如下表所示: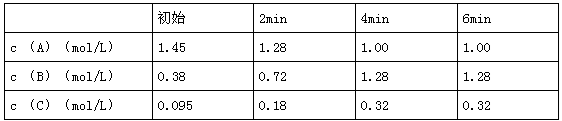
下列说法正确的是:
A.该反应的化学方程式为A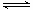 2B+C
2B+C
B.4min末A的转化率约为31%
C.4~6min时,反应停止了
D.正反应是吸热反应
将100mL1L•mol-1的NaHCO3溶液分为两份,其中一份加入少许冰醋酸,另外一份加入少许Ba(OH)2固体,忽略溶液体积变化。两份溶液中c(CO32-)的变化分别是()
| A.减小、减小 | B.增大、减小 | C.增大、增大 | D.减小、增大 |