下列有关热化学方程式的叙述中,正确的是( )
| A.含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则表示该反应中和热的热化学方程式为 NaOH(aq)+HCl(aq) =NaCl(aq)+H2O(l)ΔH=+57.4 kJ/mol |
| B.已知C(石墨,s) =C(金刚石,s)ΔH>0,则金刚石比石墨稳定 |
| C.已知2H2(g)+O2(g) =2H2O(g) ΔH=-483.6 kJ/mol,则H2燃烧热为241.8 kJ/mol |
| D.已知2C(s)+2O2(g) =2CO2(g) ΔH1,;2C(s)+O2(g) =2CO(g)ΔH2;则ΔH1<ΔH2 |
一定量的CuS投入足量的HNO3中,收集到标准状况下的气体VL,向反应后的溶液中加入足量的NaOH,产生蓝色沉淀,经过滤、洗涤、灼烧,得到CuO 12g,若上述气体为NO和NO2的混合物,且体积比为1∶1,则V为
| A.9.0L | B.13.44L | C.15.7L | D.16.8L |
一定条件下硝酸铵受热分解的化学方程式为:5NH4NO3=2HNO3+4N2+9H2O,在反应中被氧化与被还原的氮原子数之比为
| A.5∶3 | B.5∶4 | C.1∶1 | D.3∶5 |
根据转化关系判断下列说法正确的是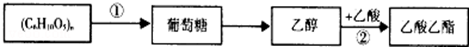
| A.(C6H10O5)n可以是淀粉或纤维素,二者均属于多糖,互为同分异构体 |
| B.可以利用银镜反应证明反应①的最终产物为葡萄糖 |
| C.酸性高锰酸钾可将乙醇氧化为乙酸,将烧黑的铜丝趁热插乙醇中也可得到乙酸 |
| D.在反应②得到的混合物中倒入饱和氢氧化钠溶液并分液可得到纯净的乙酸乙酯 |
下列反应属于取代反应的组合是
①CH3CH=CH2+Br2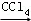 CH3CHBrCH2Br
CH3CHBrCH2Br
②CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
③2CH3CH2OH+O2 2CH3CHO+2H2O
2CH3CHO+2H2O
④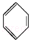 +Br2
+Br2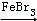
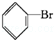 +HBr.
+HBr.
| A.①② | B.③④ | C.①③ | D.②④ |
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电.其电池反应为:2CH3OH+3O2+4OH﹣ 2CO32﹣+6H2O,则下列说法错误的是()
2CO32﹣+6H2O,则下列说法错误的是()
| A.放电时CH3OH参与反应的电极为正极 |
| B.充电时电解质溶液的pH逐渐增大 |
| C.放电时负极的电极反应为:CH3OH﹣6e﹣+8OH﹣=CO32﹣+6H2O |
| D.充电时每生成1molCH3OH转移6mol电子 |