下面四个选项是四位同学在学习过化学反应速率理论和化学平衡理论以后,联系化工生产实际所发表的看法,你认为不正确的是( )
| A.化学反应速率理论可指导怎样在一定时间内快出产品 |
| B.化学平衡理论可指导怎样使用有限原料多出产品 |
| C.化学反应速率理论可指导怎样提高原料的转化率 |
| D.正确利用化学反应速率和化学平衡理论都可提高化工生产的综合经济效益 |
下列有关物质的性质或应用说法不正确的是
| A.可用FeCl3溶液除去试管内壁上的难以刷去的铜迹 |
| B.浓硫酸能干燥氯气、一氧化碳等气体,说明浓硫酸具有吸水性 |
| C.二氧化硫具有漂白性,所以能使溴水和品红溶液褪色 |
| D.福尔马林、葡萄糖溶液与新制氢氧化铜悬浊液共热,都会有砖红色沉淀产生 |
下列有关化学用语的表达正确的是
A.甲醛的电子式: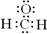 |
B.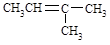 的名称:3―甲基―2―丁烯 的名称:3―甲基―2―丁烯 |
C.含78个中子的碘的放射性核素: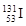 |
| D.纯碱溶液呈碱性的原理:CO32-+2H2O=H2CO3+2OH- |
中央电视台报道,一种名叫“排毒基强离子排毒仪”的产品正在市场热销。向排毒盆内倒入了纯净的温水,双脚放入盆中,启动电源开关,加入了适量精盐。过一段时间,盆中开始出现绿色、红褐色的絮状物。下列说法正确的是
| A.此“排毒基强离子排毒仪”一定是用惰性电极制成的 |
| B.加一些精盐的主要目的是起到消炎杀菌的作用 |
| C.绿色、红褐色的絮状物就是从脚底排出的体内毒素 |
| D.绿色、红褐色的絮状物是氢氧化亚铁、氢氧化铁形成的混合物 |
甲试管中盛有0.5mol/L Na2CO3溶液10mL,慢慢往试管中加入1mol/L的盐酸7.0mL;乙试管中盛有1mol/L的盐酸7.0mL,慢慢往试管中滴加0.5mol/L Na2CO3溶液10mL,那么甲、乙两试管中产生的CO2物质的量大小关系为()
| A.甲=乙 | B.甲>乙 | C.甲<乙 | D.无法确定 |
将氯化铝溶液和氢氧化钠溶液等体积混合,得到的沉淀物中含铝元素的质量与溶液中铝元素的质量相等,则原氯化铝溶液和氢氧化钠溶液的物质的量浓度之比可能是()
| A.1:3 | B.2:5 | C.1:4 | D.2 :7 :7 |