有一种自生氧防毒面具,其使用的生氧剂的主要成分是KO2。某研究小组取100 g生氧剂放入装置A中,加入足量水使之充分反应(4KO2+2H2O=4KOH+3O2↑),测定反应前后装置A的总质量。他们进行了三次实验,测定结果如下:
| 测定序号 |
第1次 |
第2次 |
第3次 |
平均值 |
| 反应前装置A总质量(g) |
400.1 |
400.2 |
399.7 |
400.0 |
| 反应后装置A总质量(g) |
376.1 |
376.1 |
375.8 |
376.0 |
请根据上述实验结果计算:(假设杂质不含钾元素且不与水反应)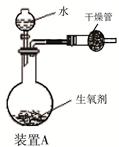
(1)100 g 生氧剂与水反应生成的氧气质量;
(2)生氧剂中含钾元素的质量分数。
某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁,他们为了测定水垢中碳酸钙的含量,取某种稀盐酸100 g加入到15.8 g水垢中,产生CO2气体的情况如下图所示。计算: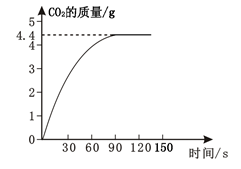
(1)从图中可以看出15.8 g水垢与盐酸反应后生成CO2最多是 。
(2)水垢中碳酸钙的质量分数是多少?(计算结果保留0.1%)
(3)所用稀盐酸中溶质质量分数是多少?(计算结果保留0.1%)
为了测定石灰石中碳酸钙的质量分数,某兴趣小组的同学称取石灰石样品12.5g,高温煅烧至质量不再改变,称得剩余固体质量为8.1g(假设杂质不参加反应;发生反应的化学方程式为CaCO3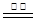 CaO+CO2↑),试计算:
CaO+CO2↑),试计算:
(1)生成二氧化碳质量是__________g;
(2)石灰石样品中碳酸钙的质量分数是多少?(写出计算过程)
已知金属钠能与水发生如下反应:2Na+2H2O═2NaOH+H2↑,若把4.6g金属钠投入到盛有足量水的烧杯中(如图),充分反应后烧杯中剩余溶液质量是40g,请计算:
(1)生成NaOH的质量.
(2)反应后所得NaOH溶液的溶质质量分数.
热水瓶用久后,瓶胆内壁常附着一层水垢(主要成份是CaCO3和Mg(OH)2,其它成份忽略不计).某兴趣小组的同学为了探究水垢中Mg(OH)2的含量,取10g水垢样品,向样品中加入足量的稀盐酸,其变化关系如图所示,试计算:
(1)生成二氧化碳的质量为 克.
(2)该水垢样品中Mg(OH)2的质量分数.(写出解题步骤)
人体胃酸过多会引起胃病。右图为某抗酸药包装标签上的部分文字,请回答下列问题。
(1)Al(OH)3的相对分子质量为 。
(2)经测定,每片该抗酸药实含氢氧化铝234mg。计算一片该抗酸药可消耗7.3%的盐酸多少克(请写出计算过程)?