工业上用固体硫酸亚铁制取颜料铁红(Fe2O3),反应原理是: 
2FeSO4 Fe2O3 + SO2↑+SO3↑,某学生欲检验该反应所产生的气态物质,他依次将气体通过盛有(I)BaCl2溶液、(II)x溶液、(III)NaOH溶液的三个装置。则下列对该方案的评价中正确的是( )
| A.(I)中会生成BaSO3、BaSO4两种沉淀 |
| B.可将(I)中的BaCl2溶液改为Ba(NO3)2溶液 |
| C.(III)的作用是检验生成的SO2气体 |
| D.(II)所盛x应为品红溶液 |
以下电子排布式是基态原子电子排布式的是( )
| A.1s12s1 |
| B.1s22s22p63s23d1 |
| C.1s22p1 |
| D.1s22s22p1 |
A、B、C、D、E是核电荷数依次增大的五种短周期元素,原子半径按D、E、B、C、A的顺序依次减小,B和E同主族,则下列推断中不正确的是( )
A.A、B、E一定各在不同周期
B.A、D可能在同一主族
C.C的最高正价氧化物对应的水化物可能显碱性
D.C和D的单质可能化合形成离子化合物
下列外围电子排布式(或外围轨道表示式)的原子中,第一电离能最小的是( )
A.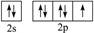 |
B.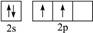 |
| C.3d64s2 | D.6s1 |
X与Y两元素的阳离子具有相同的电子层结构,X元素的阳离子半径大于Y元素的阳离子半径,Y与Z两元素的核外电子层数相同,Z元素的第一电离能大于Y元素的第一电离能,则X、Y、Z的原子序数( )
| A.X>Y>Z |
| B.Y>X>Z |
| C.Z>X>Y |
| D.Z>Y>X |
下列说法中错误的是( )
| A.所有的非金属元素都分布在p区 |
| B.元素周期表中ⅢB族到ⅡB族10个纵行的元素都是金属元素 |
| C.除氦以外的稀有气体原子的最外层电子数都是8 |
| D.同一元素的各种同位素的化学性质一定相同 |