高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比C12、O2、C1O2、KMnO4氧化性更强,消毒杀菌能力更强,且无二次污染;工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:
2FeSO4+6Na2O2 ="=" 2Na2FeO4+2Na2O+2Na2SO4+O2↑
①该反应中的氧化剂是 ,还原剂是 ,每生成1mo1Na2FeO4转移电子的数目为
②简要说明K2FeO4,作为水处理剂时,在水处理过程中所起的作用 (2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、C1O-、OH-、FeO42-、C1-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式:
②每生成1 mo1 FeO42-转移 mo1电子,若反应过程中转移了0.3mo1电子,则还原产物的物质的量为 mo1。
③低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明 。
⑴写出金属钾与水反应的离子方程式 ▲ ;
⑵写出苯发生硝化反应的化学方程式 ▲ ;
⑶将一根亮红色的铜丝放置于酒精灯外焰上加热,然后由外焰逐渐向内焰处移动,发现铜丝由亮红色转化为黑色,进入火焰的内焰后铜丝黑色又转化为亮红色。写出黑色转化为亮红色这一现象所发生反应的化学方程式 ▲ 。
A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中A、C及B、D分别是同主族元素。又知B、D两元素的原子核中质子数之和是A、C两元素的原子核中质子数之和的2倍。这四种元素的单质中常温下有两种是气体,其中一种气体易燃烧,另外两种为固体,其中一种是黄色晶体,质脆,易研成粉末。
⑴写出元素符号:A ▲ B ▲ C ▲ D ▲ 。
⑵写出两种均含A、B、C、D四种元素的化合物相互反应放出气体的化学方程式:
▲ 。
⑶用电子式表示化合物C2D形成过程 ▲ 。
⑷用A和B两元素的单质可以制成燃料电池,电池中装有浓KOH溶液。用多孔的惰性电极浸入浓KOH溶液中,两极均有特制的防止气体透过隔膜,在一极通入A的单质,另一极通入B的单质。写出通入B单质的一极电极反应式是: ▲ 。
(8分)在下列各组物质中,找出合适的序号填在对应的空格内:
①NO2和N2O4 ②12C和14C ③
④
⑤ ⑥甲烷与丙烷
⑥甲烷与丙烷
⑦乙醇(CH3CH2OH)和乙二醇(HO—CH2—CH2—OH)
注意:以上七组物质,不一定是每组物质都能找到对应填空
⑴互为同位素的是 ▲ ;⑵互为同分异构体的是 ▲ ;
⑶互为同系物的是 ▲ ;⑷同一种物质的是 ▲ 。
已知蓝铜矿的主要成分是2CuCO3·Cu(OH)2,受热易分解。铝土矿的主要成分是Al2O3、Fe2O3、SiO2。经过一定条件的转化二者均可转化为金属单质,根据下列框图转化回答问题: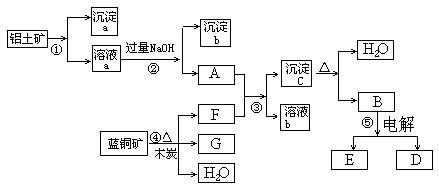
(1)写出①的离子方程式:______________________、_____________________。
(2)经过④、⑤步反应得到铜和金属铝,写出反应的化学方程式:
_____________________、______________________。
(3)若过量F与A反应,溶液b的成分是:______(写化学式)。
有机物A(C6H8O4)为食品包装纸的常用防腐剂。A可以使溴水褪色。A难溶于水,但在酸性条件下可发生水解反应,得到B(C4H4O4)和甲醇。通常状况下B为
无色晶体,能与氢氧化钠溶液发生反应。
(1)A可以发生的反应有(选填序号)。
① 加成反应 ② 酯化反应 ③ 加聚反应 ④ 氧化反应
(2)B分子中没有支链,其结构简式是
(3)由B制取A的化学方程式是。