下列离子方程式正确的是
| A.铁与稀硫酸反应:2Fe + 6H+ = 2Fe3﹢ +3H2↑ |
| B.Al(OH) 3沉淀中滴加盐酸Al(OH)3 + H﹢ = Al3﹢+H2O |
| C.碳酸氢钠溶液中加入稀盐酸:HCO3- +H+= CO2 ↑ +H2O |
| D.碳酸钙与稀盐酸反应:CO32- + 2H+= CO2↑ + H2O |
下列关于判断过程的方向的说法正确的是 ( )
| A.所有自发进行的化学反应都是放热反应 |
| B.判断化学反应能否自发进行,必须综合考虑反应的焓变和熵变 |
| C.自发反应一定是熵增大,非自发反应一定是熵减小的反应 |
| D.同一物质的固、液、气三种状态中固体的熵值最大 |
如图是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列有关的判断正确的是( )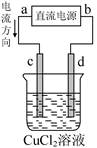
| A.a为负极、b为正极 |
| B.a为阳极、b为阴极 |
| C.电解过程中,d电极质量增加 |
| D.电解过程中,氯离子浓度不变 |
对于反应2CO(g)+ O2(g) 2CO2(g)(正反应为放热反应),在一定条件下建立化学平衡后,下列各条件变化时,能使平衡正向移动的是 ( )
2CO2(g)(正反应为放热反应),在一定条件下建立化学平衡后,下列各条件变化时,能使平衡正向移动的是 ( )
| A.恒容通入少量He | B.恒容通入少量CO2 | C.升高温度 | D.缩小容器体积 |
下列反应属于吸热反应的是 ( )
| A.中和反应 | B.锌与稀硫酸反应 |
| C.炭燃烧生成CO | D.炭与高温水蒸汽反应 |
合理利用燃料减小污染符合“绿色奥运”理念,下列关于燃料的说法正确的是( )
| A.“可燃冰”是将水变为油的新型燃料 |
| B.氢气是具有热值高、无污染等优点的燃料 |
| C.乙醇是比汽油更环保、不可再生的燃料 |
| D.石油和煤是工厂经常使用的可再生的化石燃料] |