铜锌原电池(如图)工作时,下列叙述错误的是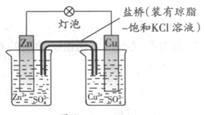
| A.正极反应为:Cu2++2e–= Cu |
| B.电池反应为:Zn+Cu2+=Zn2+ +Cu |
| C.在外电路中,电子从负极流向正极 |
| D.盐桥中的K+移向ZnSO4溶液 |
CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是
| A.相对于途径①,途径②更好地体现了绿色化学思想 |
| B.Y可以是葡萄糖溶液 |
| C.CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体 |
| D.将CuSO4溶液蒸发浓缩,冷却结晶可制得胆矾晶体 |
关于下列各装置图的叙述中,正确的是



① ② ③ ④
| A.实验室用装置①制取氨气 |
| B.装置②可用于制备氢氧化亚铁并观察其颜色 |
| C.装置③中X为苯,可用于吸收氨气,并防止倒吸 |
| D.装置④是原电池,锌电极为负极,发生氧化反应 |
如下图所示,△H1=-393.5 kJ•mol-1,△H2=-395.4 kJ•mol-1,下列说法正确的是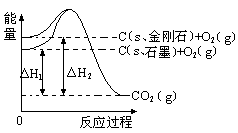
| A.1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ |
| B.石墨和金刚石的转化是物理变化 |
| C.金刚石的稳定性强于石墨 |
| D.C(s、石墨)==C(s、金刚石) △H=" +1.9" kJ•mol-1 |
汽车的启动电源常用铅蓄电池,放电时的电池反应如下:PbO2 +Pb+2H2SO4=2PbSO4+2H2O,根据此反应判断下列叙述中正确的是
| A.PbO2是电池的负极 | B.负极的电极反应式为:Pb+SO42--2e– = PbSO4 |
| C.PbO2得电子,被氧化 | D.电池放电时,溶液酸性增强 |
右图为元素周期表中短周期的一部分,下列说法正确的是
| A.非金属性:Y>Z>M |
| B.离子半径:M->Z2->Y- |
| C.ZM2分子中各原子的最外层均满足8电子稳定结构 |
| D.三种元素中,Y的最高价氧化物对应的水化物酸性最强 |