小明通过有关资料得知在宇宙飞船上可以安装盛有Na2O2(过氧化钠)的装置,它的作用是与人呼出的二氧化碳反应生成氧气。于是他进行以下的探究活动: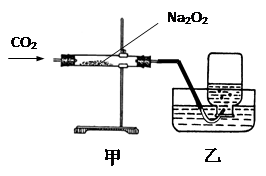
(1)他用右图装置制取并收集一瓶氧气,为检验收集到的氧气中是否含有二氧化碳,他应向集气瓶中滴入 ,振荡,发现 ,证明他收集到的氧气中还含有CO2。为使他能收集到一瓶较为纯净的氧气,你认为他应在甲、乙装置中间再连接以下的哪个装置? 。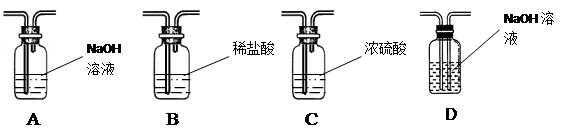
(2)进一步探究反应后玻璃管中剩余白色固体的成分。
【进行猜想】提出两个猜想:猜想①:白色固体含有过氧化钠;猜想②:白色固体含碳酸钠。
【查阅资料】过氧化钠为白色粉末,溶于水生成氢氧化钠和氧气。
【实验探究】下面是对白色固体进行实验探究的实验报告,请填写表中空白。
| 实验目的 |
操作方法 |
实验现象 |
实验结论 |
| 检验白色固体是否含有过氧化钠。 |
1、取该少量白色固体于试管里,加入适量的水; 2、用带火星的木条放在试管口。 |
1、 ; 2、 。 |
白色固体加入水后有 生成,白色固体含过氧化钠。 |
| 。 |
取该少量白色固体于试管里,向试管中滴 。 |
。 |
白色物质中含有碳酸钠。 |
【实验反思】①过氧化钠与二氧化碳反应的化学方程式是: 。
②过氧化钠常用于潜水艇、宇宙飞船上制取氧气的优点是(答2点) , 。
某化学兴趣小组在学习氧气的制法后进行一系列探究活动。
探究1.
利用如图实验装置制取氧气。
(1)写出用A装置制取氧气的化学方程式________。
探究2.
(2)小组对过氧化氢分解时影响反应速率的部分因素作出探究,并测得相关实验数据。如表:
从实验③和④对比可知,化学反应速率与________有关。通过实验________与实验________(填实验序号)对比可知,化学反应速率与反应物的浓度有关。若用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,加适量水稀释,产生氧气的总质量________。(选填“减小”或“不变”或“增大”)。
探究3.
小组中小童同学取15%的H2O2溶液5mL于试管中,加热后,观察到溶液中产生较多气泡,他直接将带火星的木条伸入试管中,木条却没有复燃,直至溶液沸腾,也未见木条复燃。小组一起反复实验讨论并通过查找资料找到了木条不能复燃的原因。
(3)有关小童在实验中带火星的木条没有复燃,下列说法中正确的有________。
| A.实验所用的过氧化氢溶液的浓度太小。 |
| B.加热过氧化氢能分解,但反应速率较慢,试管中氧气含量较少。 |
| C.加热过氧化氢溶液的同时,溶液中的水蒸气随氧气一起逸出,环境湿度较大,木条不能复燃。 |
| D.小童采用排水法去收集产生的气体,再用带火星木条检验,木条能复燃。 |
工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4。为了测定铁红中铁的质量分数,兴趣小组的同学进行了如下实验,请你参与过程分析。
【资料1】草酸晶体(H2C2O4·3H2O)在浓H2SO4作用下受热分解,化学方程式为:
H2C2O4·3H2O CO2↑+CO↑+4H2O
CO2↑+CO↑+4H2O
(1)下列可用作草酸分解制取气体的装置是(填字母编号)。
【资料2】碱石灰是氢氧化钠和氧化钙的混合物,可以吸收水分和二氧化碳;
【资料3】浓硫酸具有吸水性,可以干燥气体;
【资料4】氢氧化钠溶液和石灰水类似都可以与二氧化碳反应,但吸收能力比石灰水强
【问题讨论】用下图所示装置进行实验:
(2)实验前应先。
(3)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是(填字母编号)。
a.浓硫酸 b.澄清的石灰水c.氢氧化钠溶液
(4)B装置的作用是。
(5)写出D装置中所发生反应的一个化学方程式。
【数据分析与计算】
【资料5】铁的常见氧化物中铁的质量分数:
| 铁的氧化物 |
FeO |
Fe2O3 |
Fe3O4 |
| 铁的质量分数 |
77.8% |
70.0% |
72.4% |
(6)称取铁红样品10.0 g,用上述装置进行实验,测定铁红中铁的质量分数。
①D中充分反应后得到Fe粉的质量为m g,则 < m <。
②待充分反应、冷却后,将D中的固体放入足量的稀硫酸溶液中,产生氢气质量为0.27g,则此铁红样品中铁的质量分数是多少?[写出详细计算过程]
【实验评价】
(7)反思:请指出【问题讨论】中实验装置的一个明显缺陷。
某校初三化学学习小组的同学前往某地的石灰石矿区进行调查,他们取回矿石样品,对样品中的碳酸钙的质量分数进行检测,采用了以下的办法:
甲组同学:
测定某石灰石样品中碳酸钙的质量分数,其方法是:将样品与稀盐酸反应,测定反应后生成CO2的体积,再根据体积换算为质量,最后根据CO2的质量求出样品中碳酸钙的质量。下图为大理石与稀盐酸反应的反应装置,并测量CO2的体积。(其他仪器省略)
(1)上图中左侧的橡皮管的作用。
(2)上图中装置中油层的作用是。
(3)(填操作方法)可使反应前后油层上方气体压强和外界大气压相同,此时排出水的体积即为生成二氧化碳的体积。
乙组同学:
【查阅资料】1.氢氧化钠溶液可以吸收二氧化碳气体
2.碱石灰可以吸收二氧化碳气体和水分
取样品,研成粉状后,按下图进行实验。
(1)实验步骤:
①连接好装置,检查气密性;
②打开弹簧夹C,在A处缓缓通入一段时间空气;
③称量F的质量;
④关闭弹簧夹C,慢慢滴加稀盐酸至过量,直至D中无气泡冒出;
⑤打开弹簧夹C,再次快速通一段时间空气;
⑥称量F的质量,计算前后两次质量差。最后根据CO2的质量求出样品中碳酸钙的质量
(2)问题探究:
①产品研成粉状的目的;
②B装置的作用是;
G装置的作用是。
③若没有E装置,则测定的CaCO3的质量分数会(填“偏大 偏小 不变”)。
④在步骤②打开弹簧夹C,在A处缓缓通入一段时间空气的目的 。
总结反思:
(1)甲组同学们认为即使排除实验仪器和操作的影响,测定的结果仍不一定准确,甲组中,可能造成实验结果与真实值相比偏小的原因
(2)在乙组实验步骤中,可能造成实验结果与真实值相比偏大的原因。
现有火柴、一张干燥的白纸、一个洁净干燥的小烧杯,澄清的石灰水。证明纸张里所含元素。
[提出问题]:白纸燃烧就是跟氧气反应,生成什么物质?白纸里含什么元素?
[假设与猜想]:纸张中含碳、氢两种元素。
[设计实验]:物质燃烧,有水生成,证明物质中含氢元素;有使石灰水变浑浊的气体产生,证明物质中含有碳元素。
[实验、分析与论证、结论]
| 实验步骤 |
实验现象 |
结论 |
| (1)将白纸撕成条点燃后,将 _________________________ |
||
| (2)过一会儿,___________ __________________________ |
[反思与评价]:水和二氧化碳中都含有氧元素,该实验______(填“能”或“不能”)证明白纸中含有氧元素?理由是____________________。
草酸(C2H2O4)的化学性质与碳酸相似.已知碳酸易分解,草酸在受热条件下仅分解成三种氧化物.某学习小组对此展开探究:
(1)小明首先根据草酸中含有氢元素,可推测生成物中含有.
(2)小明对分解生成的其他产物进行猜测、验证:
【假设一】生成物中有二氧化碳
实验一:将生成的气体通入澄清的石灰水,实验现象是,小明据此判断生成物中含有二氧化碳.
【假设二】生成物中有一氧化碳
实验二:小明用下图装置进行实验,从而证明生成物中含有一氧化碳.已知A装置中黑色固体粉末是氧化铜,则 A装置中的实验现象是,A中的化学方程式为.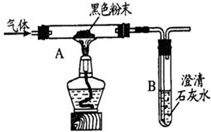
(3)讨论交流:小芳认为,从环保的角度看,“实验二”装置有一个缺陷,请你指出处理方法一:,处理方法二.:.
(4)写出草酸在受热分解的化学方程式:.