写出下列方程式:(注明反应的条件,并配平方程式)
① 实验室制乙炔
② 乙烯与水反应
③ 乙烷与氯气生成一氯乙烷
④ 1,3 – 丁二烯与氯气发生1,4 – 加成
⑤ 甲苯与浓硝酸反应
6.02×1024个Mg约含mol Mg,其质量为g;49gH2SO4约含有
个H原子,共含有 _____mol原子。
填空
| 物质 |
分子数 |
质量/g |
物质的量/mol |
摩尔质量/g.mol-1 |
| O2 |
8.0 |
|||
| H2SO4 |
3.01×1023 |
|||
| H2O |
0.5[ |
写出下列物质的电离方程式:
HNO3 Ba(OH)2
Na3PO4
A、B、C、D四种芳香族化合物都是某些植物挥发油中的主要成分,有的是药物,有的是香料。它们的结构简式如下所示: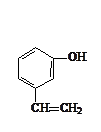
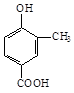
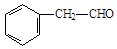
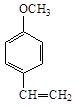
A BC D
回答下列问题:
(1)化合物C的分子式为 ,C中的含氧官能团名称是。
(2)1molB最多能与molH2发生反应,B与新制Cu(OH)2反应的产物的结构简式
为。
(3)D发生聚合反应的产物的结构简式为。
(4)A能与乙醇发生反应生成一种有特殊香味的物质,请写出该反应的方程式:
(5)关于上述四种物质的说法中正确的是
A.都能与Na反应放出H2
B.C、D均能使溴的四氯化碳溶液褪色
C.A和C均能与NaHCO3溶液反应放出CO2
D.1molC最多能与4molBr2发生反应
有A、B、C、D、E五种短周期元素,其元素特征信息如下表
| 编号 |
元素特征信息 |
| A |
其单质是密度最小的物质。 |
| B |
阴离子带两个单位负电荷,单质是空气的主要成分之一。 |
| C |
其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物。 |
| D |
其氢氧化物和氧化物都有两性,与C同周期 |
| E |
与C同周期,原子半径在该周期最小 |
(1)E元素的名称是。
(2)A、B、C形成的化合物的电子式为,该化合物中含有的化学键是。
(3)B、C、D的简单离子半径由大到小的顺序是(用离子符号表示)。
(4)①E单质与A、B、C形成的化合物反应的化学方程式为 ;
;
②D单质与A、B、C形成的化合物的水溶液反应的离子方程式为
;
③B、C元素形成的两种化合物与A2B反应的两个化学方程式:
、