下列有关电解质溶液中微粒的物质的量浓度关系正确的是
| A.常温下,pH=5的NaHSO3溶液中:c(HSO3一)>c(SO32一)>c(H2SO3) |
| B.在0.1mol·L一1NaHCO3溶液中有: c(Na+) +c(H+)=c(HCO3一) + c(CO32-) + c(H2CO3) |
| C.在0.1mol·L一1Na2CO3溶液:c((HCO3-) + 2c(H2CO3) +c(H+)=c(OH-) |
| D.常温下,将10mL0.lmol.L一1的盐酸与20mL0.1mol.L一1的氨水混合,所得溶液中:. |
c(NH3·H2O)>c(Cl一)>c(NH4+)>c(OH一)>c(H+)
常温下,在溶液中可发生以下反应:
①H++Z-+XO4-=== X2++Z2+H2O(未配平),
②2M2++R2===2M3++2R-,
③ 2R-+Z2=== R2+2Z-
由此判断下列说法正确的是
| A.常温下反应2M2++Z2===2M3++2Z-不可以自发进行 |
| B.R元素在反应②中被氧化,在③中被还原 |
| C.反应①配平后,H2O的化学计量数为8 |
| D.还原性强弱顺序为:X2+>Z->R->M2+ |
下列离子组在一定条件下能共存,当加入相应试剂后会发生化学变化,且所给离子方程式正确的是
| 选项 |
离子组 |
加入试剂 |
加入试剂后发生反应的离子方程式 |
| A |
Fe2+、NO3-、K+ |
稀硫酸 |
3Fe 2++NO3-+4H+===3Fe3++NO↑+2H2O |
| B |
Fe3+、I-、ClO- |
氢氧化钠溶液 |
Fe3++3OH-===Fe(OH)3↓ |
| C |
Ba2+、HCO3-、Cl- |
氢氧化钠溶液 |
HCO3-+OH-===CO32-+H2O |
| D |
Al3+、Cl-、NO3- |
过量氢氧化钠溶液 |
Al3++3OH-===Al(OH)3↓ |
在下述条件下,一定能大量共存的离子组是
| A.无色透明的水溶液中:K+、Ba2+、I-、MnO4- |
| B.含有大量NO3-的水溶液中:NH4+、Fe2+、SO42-、H+ |
| C.C(HCO3-)=0.1 mol·L-1的溶液中:Na+、K+、CO32-、Br- |
| D.强碱性溶液中:ClO-、S2-、HSO3-、Na+ |
下列实验设计及其对应的离子方程式均正确的是
| A.用FeCl3溶液腐蚀铜线路板:Cu + 2Fe3+= Cu2+ + 2Fe2+ |
| B.Na2O2与H2O反应制备O2:Na2O2 + H2O= 2Na+ + 2OH-+ O2↑ |
| C.将氯气溶于水制备次氯酸:Cl2 + H2O= 2H+ + Cl-+ ClO- |
D.用惰性电极电解饱和氯化钠溶液:2Cl- + 2H+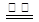 H2↑+ Cl2↑ H2↑+ Cl2↑ |
图表归纳是学习化学的一种常用方法,某同学如下归纳的下表与上图中对应正确的是
| 选项 |
X |
Y |
Z |
 |
| A |
胶体 |
混合物 |
淀粉溶液 |
|
| B |
化合物 |
酸性氧化物 |
一氧化氮 |
|
| C |
气态氢化物 |
化合物 |
液溴 |
|
| D |
强电解质 |
强酸 |
硫酸 |