下列说法正确的是( )
| A.若把H2S分子写成H3S分子,违背了共价键的饱和性 |
| B.H3O+离子的存在,说明共价键不应有饱和性 |
| C.所有共价键都有方向性 |
| D.两个原子之间形成共价键时,可形成多个σ键 |
下列有关物质的性质或应用均正确的是
| A.二氧化硅为酸性氧化物,可用于制作计算机芯片 |
| B.氢氧化镁分解时吸收大量的热量,添加到合成树脂中可作阻燃剂 |
| C.碳酸钠可以作为食品疏松剂 |
| D.食品工业中可以用二氧化硫加工银耳,使之更白 |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.使苯酚显紫色的溶液:NH4+、K+、SCN-、NO3- |
| B.澄清透明的溶液:Cu2+、Mg2+、SO42-、Cl- |
| C.0.1 mol·L-1 Na2CO3溶液:NH4+、Fe2+、SO42-、NO3- |
| D.c(Fe2+)=1.0 mol·L-1溶液:H+、K+、Cl-、MnO4- |
下列有关化学用语表述正确的是
A.S2-的结构示意图: |
B.CO2的比例模型: |
C.邻羟基苯甲酸的结构简式: |
| D.质子数为79、中子数为118的金(Au)原子:118 79Au |
化学与生产、生活、环境保护等密切相关。下列叙述正确的是
| A.绿色食品是生产时不使用化肥农药,不含任何化学物质的食品 |
| B.新型材料聚酯纤维、光导纤维都属于有机高分子材料 |
| C.医药中常用酒精来消毒,是因为酒精能够使病毒的蛋白质发生变性 |
| D.CO2的水溶液呈酸性,CO2的大量排放会导致酸雨的形成 |
日用牙膏的主要成分有:活性物质、摩擦剂、甘油等。假设牙膏中摩擦剂成分为CaCO3、SiO2、Al(OH)3中的一种或几种物质组成,牙膏中其他成分均可溶于益酸,且无气体产生。
(1)牙膏中添加甘油主要作用____。
为进一步探究牙膏中摩擦剂成分,进行了以下探究:
I摩擦剂成分的定性检验:设计实验方案,验证假设。请写出实验步骤以及预期现象和结论(可不填满也可补充)。可选的试剂:稀盐酸,稀硫酸,NaOH溶液,澄清石灰水
| 实验步骤 |
预期现象和结论 |
| 步骤1:取适量牙膏样品,加水充分搅拌、过滤 |
有难溶物存在 |
| 步骤2: |
①有无色气泡产生,说明有CaCO3; ②_________,说明有______。 |
| 步骤3: |
|
| …… |
II.牙膏样品中碳酸钙的定量测定
利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。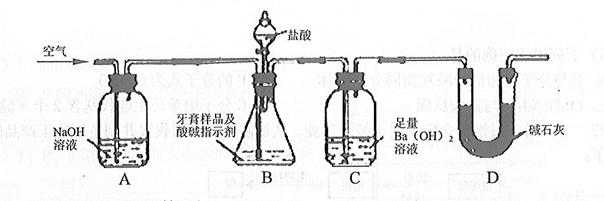
依据实验过程回答下列问题:
(2)实验过程中需持续缓缓通入空气。其主要作用 。
(3)仪器C中选择Ba(OH)2而不选择Ca(OH)2溶液原因:① 。② 。
(4)下列各项措施中,能提高测定准确度的是____(填标号)。
a.在加入盐酸之前,应排净装置内的CO2气体
b.缓慢滴加稀盐酸
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(5)实验中准确称取10.00g样品三份,进行三次测定,洌得BaCO3平均质量为3.94g。则样品中碳酸钙的质量分数为____。若改测定C中生成BaCO3质量为测定装置C在吸收CO2前后的质量差来确定CaCO3的质量分数,两方法测定的结果____(填“相同”或“不同”),原因是 。