室温时,下列混合溶液的PH一定小于7的是
| A.PH=3的盐酸和PH=11的氨水等体积混合 |
| B.PH=3的盐酸和PH=11的氢氧化钡等体积混合 |
| C.PH=3的醋酸和PH=11的氢氧化钡等体积混合 |
| D.PH=3的硫酸和PH=11的氨水等体积混合 |
分子式为C5H7Cl的有机物,其结构不可能是()
| A.只含有1个双键的直链有机物 | B.含2个双键的直链有机物 |
| C.含1个双键的环状有机物 | D.含一个三键的直链有机物 |
现有乙酸和两种链状单烯烃的混合物,若其中氧的质量分数为a ,则碳的质量分数是()
| A.6(1-a)/7 | B.3a/4 |
| C.(1-a)/7 | D.12 (1-a)/13 |
能说明苯环对羟基有影响,使羟基变得活泼的事实是()
| A.苯酚能和溴水迅速反应 | B.液态苯酚能与钠反应放出氢气 |
| C.室温时苯酚不易溶解于水 | D.苯酚具有极弱酸性 |
加热聚丙烯废塑料可以得到碳、氢气、甲烷、乙烯、丙烯、苯和甲苯。用如图所示装置探究废旧塑料的再利用。下列叙述中不正确的是() 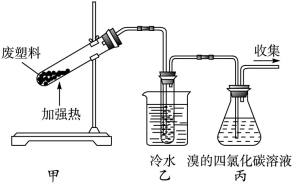
| A.聚丙烯的链节是—CH2—CH2—CH2— |
| B.装置乙的试管中可收集到芳香烃 |
| C.装置丙中的试剂可吸收烯烃以制取卤代烃 |
| D.最后收集的气体可作燃料 |
科学家艾哈迈德·泽维尔使“运用激光技术观察化学反应时分子中原子的运动”成为能,在他的研究中证实了光可诱发下列变化: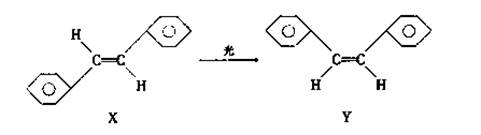
这一事实可用于解释人眼的夜视功能,有关X、Y的叙述不正确的是( )
| A.X和Y为同一种物质 |
| B.X和Y与氢气加成后生成同一种物质 |
| C.X和Y都可以发生加聚反应 |
| D.X和Y物理性质有差异 |