某酸的酸式盐NaHY在水溶液中,HY-的电离程度小于HY-的水解程度。有关的叙述正确的是
| A.H2Y的电离方程式为:H2Y |
| B.在该酸式盐溶液中:[Na+]>[Y2-]>[HY-]>[OH-]>[H+] |
C.HY-的水解方程式:HY-+H2O H3O++Y2- H3O++Y2- |
| D.在该酸式盐溶液中:[Na+]>[HY-]>[OH-]>[Y2-]>[H+] |
已知常温下Ksp(AgCl)=1.8×l0-10,Ksp(AgBr)=5×10 -13,下列有关说法错误的是
A.在饱和AgCl、AgBr的混合溶液中: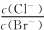 = 360 = 360 |
| B.向AgCl悬浊液中滴加浓NaBr溶液会产生淡黄色沉淀 |
| C.AgCl在水中溶解度及Ksp均比在NaCl溶液中的大 |
| D.欲用1 L NaCl溶液将0.01 mol AgBr转化为AgCl,则c(NaCl)≥3.61 mol/L |
25℃时,将某一元碱MOH和盐酸溶液等体积混合(体积变化忽略不计),测得反应后溶液的pH如下表,则下列判断不正确的是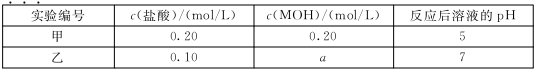
A.实验甲所得溶液: |
B.将实验甲中所得溶液加水稀释后,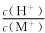 变小 变小 |
| C.a>0.10 |
D.MOH的电离平衡常数可以表示为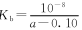 |
如图是利用一种微生物将废水中的有机物(假设是淀粉)的化学能直接转化为电能,并利用此电能在铁上镀铜,下列说法中正确的是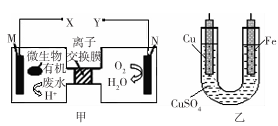
| A.质子透过离子交换膜由右向左移动 |
| B.铜电极应与X相连接 |
C.M电极反应式: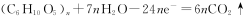 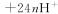 |
| D.当N电极消耗0.25 mol气体时,则铁电极增重16 g |
已知25℃时:①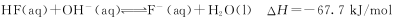
②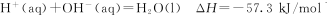 下列有关说法中正确的是
下列有关说法中正确的是
A.HF电离:HF(aq) H+(aq)+F-(aq)△H=+10.4KJ/mol H+(aq)+F-(aq)△H=+10.4KJ/mol |
| B.水解消耗0.1 mol F时,吸收的热量为6.77 kJ |
| C.中和热均为57.3 kJ/mol |
| D.含0.1 mol HF、0.1 mol NaOH的两种溶液混合后放出的热量为6.77 kJ |
原子序数依次增大的四种短周期元素X、Y、Z、W,X与Z同主族且X最外层电子比次外层电子多2个,Y元素的周期序数等于族序数,W元素的最高正价与最低负价代数和为4,下列说法错误的是
| A.最高价氧化物对应水化物的酸性:W>X>Z>Y |
| B.氢化物的稳定性:X>Z |
| C.Y单质可用于钢轨的焊接 |
| D.原子半径大小顺序:X<Y<Z<W |