CO、CH4均为常见的可燃性气体。
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是_____________。
(2)已知在101 kPa时,CO的燃烧热为283 kJ·mol-1。相同条件下,若2 mol CH4完全燃烧,生成液态水,所放出的热量为1 mol CO完全燃烧放出热量的6.30倍,CH4完全燃烧反应的热化学方程式是______________________________________。
(3)120 ℃、101 kPa下,a mL由CO、CH4组成的混合气体在b mL O2中完全燃烧后,恢复到原温度和压强。
①若混合气体与O2恰好完全反应,产生b mL CO2,则混合气体中CH4的体积分数为_____________(保留2位小数)。
②若燃烧后气体体积缩小了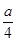 mL,则a与b关系的数学表示式是____________。
mL,则a与b关系的数学表示式是____________。
甲、乙、丙、丁、戊为原子序数依次增大的短周期元素。甲、丙处于同一主族,丙、丁、戊处于同一周期,乙与另四种元素既不同周期也不同主族,戊原子的最外层电子数是甲、乙、丙原子最外层电子数之和。甲、乙组成的常见气体X能使湿润的红色石蕊试纸变蓝;丁的单质既能与甲戊组成的化合物Y的水溶液反应产生氢气、又能与丙最高价氧化物对应的水化物Z的水溶液反应产生氢气。
请回答下列问题:
(1)X的化学式为________,X所含化学键类型为____________________。
(2)丙、丁分别是________、________(写元素符号)。
(3)丁的单质与Z的水溶液反应的离子方程式为:___________________________。
(4)用电子式表示戊元素组成的单质分子的形成过程:______________________________。
(5)X与Y能发生化合反应生成化合物W,W的化学式为___________,W是______(“离子”或“共价”)化合物。
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z是同周期中非金属性最强的元素。
(1)W原子的结构示意图为_______________。
(2)X位于元素周期表第_____周期第_____族。
(3)Y的最高价氧化物对应的水化物的化学式为__________。
(4)Z单质与溴单质相比,更易与氢气发生化合反应的是______(写化学式)。
(5)X与W能形成两种化合物,其化学式为________ 、________。
、(1)下表是部分短周期元素的原子半径及主要化合价
| 元素代号 |
L |
M |
Q |
R |
T |
| 原子半径/nm |
0.160 |
0.143 |
0.112 |
0.104 |
0.066 |
| 主要化合价 |
+2 |
+3[ |
+2 |
+6、-2 |
-2 |
①L元素的名称是______,R元素的名称是______。
②能与T元素组成的化合物具有两性的是________________(写化学式)。
(2)某种融雪剂主要成分为XY2,X、Y均为周期表中前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
①该融雪剂主要成分的化学式为__________;X与氢元素形成的化合物的电子式为____________________。
②元素D、E原子的最外层电子数是相应原子电子层数的2倍,D与Y相邻,D元素是______,E元素是______。
、下表表示元素周期表的一部分,回答下列有关问题(要求用化学用语):
| 族 周期 |
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
| 2 |
a |
b |
||||||
| 3 |
c |
d |
e |
f |
g |
h |
i |
|
| 4 |
j |
k |
(1)写出下列元素符号:d______ 、 i______。
(2)k原子的电子层数为_____,f原子最外层电子数为_____。
(3)这11种元素中,单质的化学性质最稳定的是_____。
(4)在这些元素的最高价氧化物对应的水化物中,酸性最强的是_________,碱性最强的是_________,呈两性的是_________(写化学式);
写出它们两两反应的化学方程式:
__________________________________、__________________________________
__________________________________
(5)证明c、d原子失电子能力强弱的实验方法是_____________________________________;证明g、h原子得电子能力强弱的方法(用离子方程式表示)是_________________________________。
、现有A、B、C、D四种金属片,①把A、B用导线连接后同时浸入稀硫酸中,A上有气泡;②把C、D用导线连接后同时浸入稀硫酸中,D发生还原反应;③把A、C用导线连接后同时浸入稀硫酸中,电子流动方向为A→导线→C。装置如图所示,根据上述情况,回答下列问题: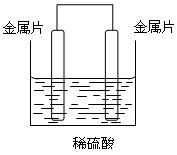
(1)四种金属的活动性顺序是_________________。
(2)在①中,金属片_____作负极;在②中,金属片_____上有气泡产生;在③中,金属片_____发生氧化反应。
(3)如果把B、D用导线连接后同时浸入稀硫酸中,则金属片_____上有气泡产生,该电极反应式为____________________。
(4)图示装置(金属片取①~③中的任一组)称为_________,它利用氧化还原反应将______能转化为______能。