把0.05 mol NaOH固体,分别加入下列100 mL溶液中,溶液的导电能力变化不大的是( )
| A.自来水 | B.0.5 mol·L-1盐酸 |
| C.0.5 mol·L-1醋酸 | D.0.5 mol·L-1 NH4Cl溶液 |
下列由相关实验现象所推出的结论正确的是
| A.向氯水中加入有色布条,片刻后有色布条褪色,说明有Cl2存在 |
| B.向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO42 |
| C.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应 |
| D.分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水 |
C、N、S都是重要的非金属元素。下列说法正确的是
A.三者对应的氧化物均为酸性氧化物
B.三者的单质直接与氧气反应都能至少生成两种氧化物
C.相同温度下,等物质的量浓度的Na2CO3、NaNO3、Na2SO3溶液的pH大小顺序:NaNO3<Na2SO3<Na2CO3
D.CO2、NO2、SO2都能与H2O反应,其反应原理相同
三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3NF3+5H2O=2NO+HNO3+9HF。下列有关说法正确的是
| A.NF3是氧化剂,H2O是还原剂 |
| B.还原剂与氧化剂的物质的量之比为2∶1 |
| C.若生成0.2 mol HNO3,则转移0.2 mol电子 |
| D.NF3在潮湿的空气中泄漏会产生红棕色气体 |
X、Y、Z、W为周期表中前20号元素中的四种,原子序数依次增大,W、Y为金属元素,X原子的最外层电子数是次外层电子数的3倍,Y、Z位于同周期,Z单质是一种良好的半导体。W能与冷水剧烈反应,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等。下列说法正确的是
| A.原子半径:W>Y>Z>X |
| B.气态氢化物的稳定性:X<Z |
| C.最高价氧化物对应水化物的碱性:Y>W |
| D.Y、Z的氧化物都有酸性和碱性 |
下列图示实验合理的是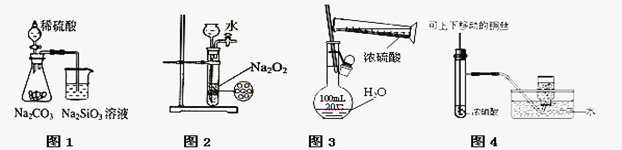
A.图1为证明非金属性强弱: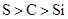 |
| B.图2为制备少量氧气 |
| C.图3为配制一定物质的量浓度的硫酸溶液 |
| D.图4为制备并收集少量NO2 |