下列各装置中都盛有0.1 mol·L—1的NaCl溶液,放置相同时间后,锌片的腐蚀速率由快到慢的顺序是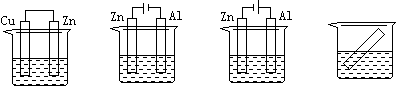
① ② ③ ④
| A.③①④② | B.①②④③ | C.②①④③ | D.②①③④ |
把锌片和铜片用导线相连后插入稀硫酸溶液中构成原电池。对该电池的描述合理的是()
①溶液中硫酸的物质的量浓度保持不变
②Cu极上有气泡产生,发生还原反应
③Cu为负极,Zn为正极
④原电池在工作时电子由负极通过溶液流向正极
⑤该装置将化学能转变为电能
| A.②⑤ | B.③⑤ | C.①② | D.④⑤ |
下列有机化学方程式书写错误的是( )
A.甲烷和氯气混合后光照:CH4+Cl2 CH3Cl+HCl CH3Cl+HCl |
B.制取氯乙烷:CH2=CH2+HCl CH2Cl-CH3 CH2Cl-CH3 |
C.制取溴苯: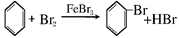 |
D.乙醇和乙酸的酯化反应:C2H5OH+CH3COOH 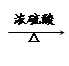 CH3COOC2H5 CH3COOC2H5 |
下列营养物质在人体内发生的变化及其对人的生命活动所起的作用叙述不正确的是( )
| A.淀粉→葡萄糖→(氧化)水和二氧化碳(释放能量维持生命活动) |
| B.纤维素(水解)→葡萄糖→(氧化)水和二氧化碳(释放能量维持生命活动) |
| C.油脂→(水解)甘油和高级脂肪酸→(氧化)水和二氧化碳(释放能量维持生命活动) |
| D.蛋白质→(水解)氨基酸→(合成)人体所需的蛋白质(人体生长发育) |
关于如图所示的氢氧燃料电池的说法错误的是()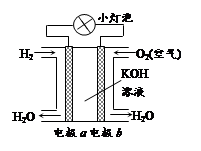
| A.电极a是负极 |
| B.电极b上的电极反应为O2+2H2O+4e-=4OH- |
| C.外电路中电子由电极b流向电极a |
| D.氢氧燃料电池的优点是高效、对环境友好 |
下列表示物质结构的化学用语或模型正确的是()
| A.乙烯的最简式:CH2=CH2 | B.CH4分子的比例模型: |
C.羟基: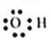 |
D.Cl-的结构示意图: |