有一瓶气体,可能是CO、CO2、H2O、H2中的一种或几种组成。为了分析该气体的成分,取适量该气体进行实验,实验方案设计如下: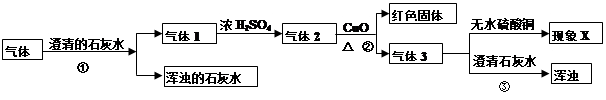
(查阅资料:白色无水硫酸铜粉末遇水变蓝色;浓H2SO4有吸水性,能干燥某些气体。)
(1)上述可能存在的气体中,易与血红蛋白结合的气体是______。
(2)实验中如果没有用浓H2SO4干燥气体1,对气体检验有无影响______。
(3)若现象X为“无水硫酸铜变蓝色”,结论是气体中 ;若现象X为“无水硫酸铜不变色”,结论是气体中 。
(4)②中一定发生的反应方程式是 。
(5)①③发生的反应相同,其反应的方程式是 。
已知A—F六种物质均为初中化学常见物质,其中B、D为氧化物,A、B、E、F为不同类别的化合物,A、B、E放入水中能使酚酞变红,下图是它们之间的关系(部分反应物和产物已省略;“→”表示转化,“—”表示相互反应),请回答:
(1)写出下列物质的化学式:B是;F可能是。
(2)写出A和E反应的化学方程式:;写出B和D反应的化学方程式:。
模拟酸雨流程如下图所示,硫在单质气体A中燃烧发出蓝紫色火焰,生成有刺激性气味的气体B,通常情况下C是无色的液体,B、C、D是氧化物,F和X是酸,G是白色沉淀。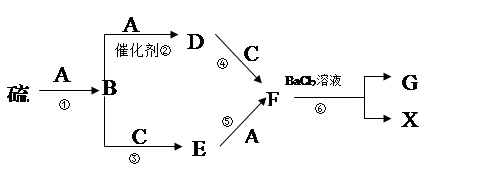
填空:⑴E的化学式
⑵反应①的化学方程式
⑶反应④的化学方程式
⑷反应⑥的化学方程式
A、B、C、D、E、F是常见的酸、碱、盐、氧化物中的一种,其中A、B是建筑材料,F是厨房中的调味品的主要成分,他们间有如下图的关系(图中 “→”表示转化关系,“—”表示相互能反应,反应条件和部分生成物省略)。回答下列问题: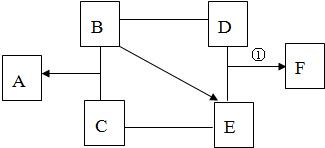
(1)A、F的化学式分别为,。
(2)C+E反应的方程式为。
(3)B+D反应的方程式为。
现有A~G七种物质,已知A是赤铁矿的主要成分, E的浓溶液稀释时会放出大量的热,G溶液为蓝色,它们之间存在如右图所示的转化关系:
(1)写出下列物质的化学式:
E:D:
F:
(2)在反应①②③中,属于置换反应的是(填序号)。
(3)工业上常利用反应①的原理来炼铁,写出反应①的化学方程式
。
(4)写出物质C与E的稀溶液发生反应的化学方程式
将一种无味的液体A装入试管,用带火星的木条试验,无现象,而向其中加入少量黑色粉末B后,迅速产生气泡,生成了使带火星的木条复燃的气体C,使金属E红热并伸入盛有气体C、瓶底有少量液体D的集气瓶中,金属E剧烈燃烧,火星四射,生成黑色固体F。
(1)写出它们的名称
A:B: C: D: E: F:
(2)黑色粉末B在A的分解反应中起作用,是这个反应的剂。
(3)写出下列化学反应的文字表达式:
①无味液体A加入少量黑色粉末B,产生气泡的反应:
②金属E在气体C剧烈燃烧,火星四射的反应: