按右图所示的方法研究某气体的性质,这种方法属于( )
| A.实验法 | B.观察法 |
| C.分类法 | D.比较法 |
下列关于日常生活中的化学问题判断正确的是
| A.为了保证食品的卫生和绿色,在食品中不能添加任何化学添加剂 |
| B.在人类必须的三大营养素糖类、油酯、蛋白质中,油酯是热能最高的营养素 |
| C.用硬水洗涤衣物时,肥皂比合成洗涤剂有更好的去污效果 |
| D.用于盛装食品的塑料袋是其主要成分是聚氯乙烯 |
物质在反应中可表现氧化性、还原性、酸性、碱性等,下面反应的划线物质中,能在同一反应中同时表现上述两种或两种以上性质的有()
①3FeO+10HNO3==3Fe(NO3)3+NO↑+5H2O②C+2H2SO4(浓)==CO2↑+2SO2↑+2H2O
③8NH3+3Cl2==6NH4Cl+N2④NaH+H2O==NaOH+H2↑⑤2Na2O2+2H2O==4NaOH+O2↑
| A.仅有①② | B.仅有①③④⑤ | C.仅有①③⑤ | D.全部 |
金属加工后的废切削液中含2-5%的NaNO2,它是一种环境污染物。人们用NH4Cl溶液来处理此废切削液,使NaNO2转化为无毒物质。该反应分两步进行:
第一步:NaNO2+NH4Cl=NaCl+NH4NO2第二步:NH4NO2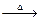 N2↑+2H2O
N2↑+2H2O
下列对第二步反应的叙述中正确的是 ()
① NH4NO2是氧化剂② NH4NO2是还原剂③ NH4NO2发生了分解反应④ 只有氮元素的化合价发生了变化⑤ NH4NO2既是氧化剂又是还原剂
| A.①③ | B.①④ | C.②③④ | D.③④⑤ |
一定温度和压强下,乙腈(CH3CN)是极易溶于水的无色液体,这时向质量分数为a的乙腈水溶液中加入等体积的水,所得溶液中乙腈的质量分数为0.4a。若同样条件下乙腈的密度为d1,水的密度为d2,则下列说法正确的是()
| A.d1<d2 | B.d1>d2 | C.d1=d2 | D.无法确定 |
Na2SO4溶液的溶解度曲线如图,下列说法一定错误的是()
A.A点表示Na2SO4溶液尚未达到饱和,但降温和加入Na2SO4·H2O晶体都可使其饱和
B.B、C点表示t1℃时,Na2SO4溶液在B点的溶解度大
于在C点的溶解度
C.在C点时Na2SO4溶液降温或升温,都会使其溶液变浑浊
D.制取芒硝的最佳方法是在100℃时配成饱和溶液,再降温至0℃析出晶体