将0.1 mol 铜与40 ml 10 mol/L HNO3充分反应后,溶液中含a mol H+,由此可知( )
| A.生成的气体在标准状况下的体积为4.48 L |
| B.生成的气体在标准状况下的体积为1.49 L |
| C.被还原的硝酸的物质的量为(0.2-a) mol |
| D.反应后溶液中所含NO的物质的量为0.2 mol |
常温时,下列叙述正确的是( )
| A.稀释pH=10的氨水,溶液中所有离子的浓度均降低 |
| B.pH均为5的HCl和NH4Cl溶液中,水的电离程度相同 |
| C.NaOH和CH3COONa的混合溶液中,c(Na+)+c(H+)=c(OH-)+c(CH3COO-) |
| D.分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多 |
25 ℃时,关于浓度均为0.2 mol/L的Na2CO3和NaHCO3溶液的说法不正确的是( )
| A.两溶液中均存在电离平衡和水解平衡 |
| B.两溶液分别加水稀释后,pH和KW均减小 |
| C.两溶液中均存在c(OH-)+2c(CO32—)+c(HCO3—)=c(Na+)+c(H+) |
| D.c(OH-)前者大于后者 |
盐MN溶于水的过程如图所示: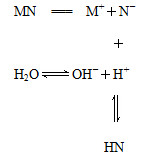
下列说法不正确的是( )
| A.MN是强电解质 |
| B.N-结合H+的能力一定比OH-强 |
| C.该过程中c(OH-)>c(H+) |
| D.溶液中存在c(HN)=c(OH-)-c(H+) |
常温下,对下列电解质溶液的有关说法一定正确的是( )
| A.相同浓度和体积的强碱和强酸溶液混合后,溶液的pH=7 |
| B.在NaHCO3溶液中,c(CO32—)>c(HCO3—) |
| C.在有AgCl沉淀的溶液中加入NaCl固体,c(Ag+)减小 |
| D.将pH相等的CH3COONa和Na2CO3溶液稀释相同倍数,CH3COONa溶液的pH较大 |
常温下,下列各组离子在有关限定条件下溶液中一定能大量共存的是( )
| A.由水电离产生的c(H+)=10-12 mol/L的溶液中:K+、Na+、ClO-、I- |
B.c(H+)=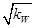 mol/L的溶液中:K+、Fe3+、Cl-、CO32— mol/L的溶液中:K+、Fe3+、Cl-、CO32— |
C.常温下,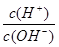 =1×10-12的溶液:K+、AlO2—、CO32—、Na+ =1×10-12的溶液:K+、AlO2—、CO32—、Na+ |
| D.pH=13的溶液中:AlO2—、Cl-、HCO3—、SO42— |