下列说法中,正确的是
| A.冰熔化时,分子中H—O键发生断裂 |
| B.原子晶体中,共价键的键长越短,键能越大,熔点就越高 |
| C.分子晶体中,共价键键能越大,该分子的熔沸点就越高 |
| D.分子晶体中,分子间作用力越大,则分子越稳定 |
下列粒子中,与NH4+具有相同质子数和电子数的是
| A.OH— | B.F- | C.Na+ | D.NH3 |
2006年10月16日美国与俄罗斯宣布,两国科学家合作成功合成了118号超重元素。对118号元素下列叙述合理的是
| A.它的最外层电子数是8 | B.它属于第VIII族 |
| C.它是活泼的金属元素 | D.它的中子数是118 |
下列有关说法,不正确的是
①将盛有二氧化氮气体的试管倒立在水中,溶液会充满试管
②酒精灯加热铝箔至熔化,铝并不滴落,因为铝表面的一层致密氧化膜熔点比铝高
③为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化
④将硅酸钠浸透的滤纸在酒精灯上灼烧,因为是湿滤纸温度低所以不能燃烧
| A.①③④ | B.②③④ | C.①③ | D.①②④ |
用下列实验装置能达到实验目的的是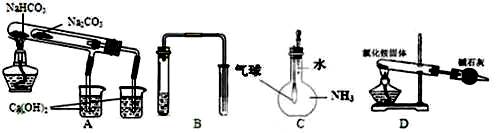
| A.比较NaHCO3和Na2CO3热稳定性大小 | B.用铜和稀硝酸制取并收集少量NO |
| C.验证氨气在水中溶解度的大小 | D.实验室用氯化铵制少量氨气 |
关于反应中的先后顺序,下列评价正确的是
| A.向浓度都为0.1mol·L-1Na2CO3和NaOH混合溶液中通入CO2,NaOH首先反应 |
| B.向NH4Al(SO4)2溶液中滴加少量的NaOH溶液,NH4+首先反应 |
| C.向浓度都为0.1mol·L-1的FeCl3和CuCl2混合溶液中加入铁粉,CuCl2首先反应 |
| D.向0.1mol·L-1的FeCl3溶液中加入质量相同、颗粒大小相同的铁和铜,铜首先反应 |