可逆反应2SO2+O2 2SO3,若用2 mol SO2和1 mol 18O2在一定条件下,经足够长的时间反应,下列情况可能出现的是
2SO3,若用2 mol SO2和1 mol 18O2在一定条件下,经足够长的时间反应,下列情况可能出现的是
| A.容器中只有三氧化硫 |
| B.18O原子存在于氧气、二氧化硫、三氧化硫中 |
| C.生成2 mol 三氧化硫 |
| D.18O原子完全存在于三氧化硫中 |
下列对对应现象的描述与离子方程式都正确的是( )
| A.金属镁与稀盐酸反应:有气体生成,Mg+2H++2Cl-=MgCl2+H2↑ |
| B.氯化钡溶液与硫酸反应:有白色沉淀生成:SO42-+Ba2+ =BaSO4↓ |
| C.碳酸钠溶液与盐酸反应:有气泡逸出:Na2CO3+2H+=2Na++CO2↑+H2O |
| D.过量铁粉与氯化铜溶液反应:溶液南蓝色变成浅绿色,同时有红色固体生成:Fe+Cu2+=Fe3++Cu |
下列反应中,既属于氧化还原反应,又属于离子反应的是( )
| A.铝片与稀盐酸的反应 |
| B.甲烷与氧气的反应 |
| C.灼热的炭与二氧化碳反应生成一氧化碳 |
| D.氢氧化钠溶液与稀盐酸的反应 |
完成下列实验所需选择的装置或仪器都正确的是( )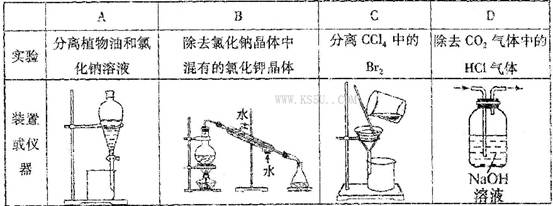
有两种体积相同的某植物的营养液,其配方如下表所示:
| KCl |
K2SO4 |
ZnSO4 |
ZnCl2 |
|
| 1 |
0.3mol |
0.2mol |
0.1mol |
- |
| 2 |
0.1mol |
0.3mol |
- |
0.1mol |
对于两种营养液的成分,下列说法中,正确的是( )
A.只有n(K+)相同B.只有n(Cl-)相同
C.各离子的物质的量均不同 D.各离子的物质的量宪全相同
铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见物质,四种物质间的反应关系如图所示。图中两圆相交部分(A、B、C、D)表示物质问的反应,其中对应的离子方程式书写正确的是( )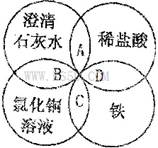
A、OH-+HCl=H2O+Cl-B、Ca(OH)2+Cu2+=Ca2++Cu(OH)2
C、Fe+Cu2+=Cu+Fe2+ D、Fe+2H+=Fe3++H2↑