长期存放的亚硫酸钠可能会被部分氧化,现通过实验来测定某无水亚硫酸钠试剂的纯度。实验步骤如下:
①称量a g样品,置于烧杯中。
②加入适量蒸馏水,使样品溶解。
③加入稀盐酸,使溶液呈强酸性,再加过量的BaCl2溶液。
④过滤,用蒸馏水洗涤沉淀。
⑤加热干燥沉淀物。
⑥将沉淀物冷却至室温后,称量。
⑦重复⑤⑥操作直到合格,最后得到b g固体。
完成下面问题:
(1)本实验中是否能用Ba(NO3)2代替BaCl2?(填“能”或“不能”)其理由是:
________________________________________________________________________。
(2)步骤③中加盐酸,使溶液呈强酸性的目的是:
____________________________________________________________________________。
(3)步骤⑦的“合格”标准是:__________________________________________________。
(4)实验测得的样品中无水亚硫酸钠的质量分数是:__________(列出算式,不需要化简)。
实验探究:探究碳、硅元素的非金属性的相对强弱
根据要求完成下列各小题
(1)实验装置:
填写所示仪器名称AB
(2)实验步骤:
连接仪器、_____________、加药品后,打开a、然后滴入浓硫酸,加热
(3)问题探究:(已知酸性强弱:亚硫酸 >碳酸)
①铜与浓硫酸反应的化学方程式是;
装置E中足量酸性KMnO4溶液的作用是;
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是;
③依据试管D中的实验现象,能否证明硫元素的非金属性强于碳元素的非金属性___(填“能”或“否”),试管D中发生反应的离子方程式是 。
。
为测定Cl2、Br2的氧化性强弱,设计了如下实验:
(可供选择的试剂有:氯水、溴水、NaCl溶液、NaBr溶液、酒精、四氯化碳)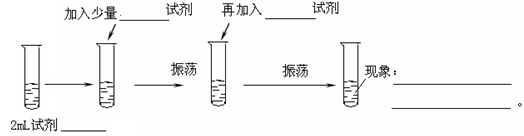
实验步骤如下:
由上回答下列问题:
(1)2ml试剂是,加入少量试剂,再加入试剂
(2)现象是。
(3)此实验可以证明Cl2的氧化性(填强于、弱于)Br2的氧化性,此反应
的离子反应方程式为:。
某自主学习小组用HNO3与大理石反应过程中质量减小的方法,探究影响反应速率的因素。所用HNO3浓度为1.00 mol·L-1、2.00 mol·L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298 K、308 K,每次实验HNO3的用量为25.0 mL,大理石用量为10.00g。
(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 |
T/K |
大理石规格 |
HNO3浓度/mol·L-1 |
实验目的 |
| ① |
298 |
粗颗粒 |
2.00 |
(Ⅰ)实验①和②探究HNO3浓度对该反应速率的影响; (Ⅱ)实验①和__探究温度对该反应速率的影响; (Ⅲ)实验①和__探究大理石规格(粗、细)对该反应速率的影响。 |
| ② |
||||
| ③ |
粗颗粒 |
|||
| ④ |
(2)实验①中CO2质量随时间变化的关系见下图:依据反应方程式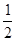 CaCO3+HNO3
CaCO3+HNO3
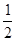 Ca(NO3)2+
Ca(NO3)2+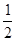 CO2↑+
CO2↑+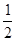 H2O,计算实验①在70-90 s范围内HNO3的平均反应速率(忽略溶液体积变化,写出计算过程)。
H2O,计算实验①在70-90 s范围内HNO3的平均反应速率(忽略溶液体积变化,写出计算过程)。
某研究性学习小组设计了一组实验来探究元素周期律。甲同学设计了如图1装置,根据元素非金属性与对应最高价含氧酸之间的关系,可以一次性完成碳族元素中C与Si的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律。A、B、C三处分别是蘸有NaBr溶液的棉花、湿润的淀粉KI试纸、蘸有碱液的棉花。已知常温下浓盐酸与高锰酸钾能反应生成氯气。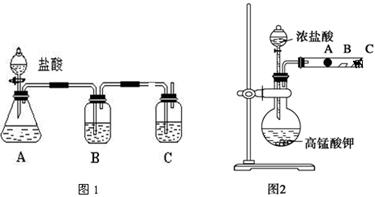
(1)甲同学设计实验的理论依据是_____________________________________;
写出选用试剂分别为:A____________,B__________,C____________;
其中装置B中所盛试剂的作用为_____________________________________;
C中反应的离子方程式为____________________________________________;
(2)乙同学的实验理论依据是______________________________________;
写出A处的离子方程式: ___________________________________________;
B处的现象,C处药品的作用。
某同学用相同质量的锌和相同浓度足量的稀盐酸反应得到实验数据如下
| 实验编号 |
锌的状态 |
反应温度/℃ |
收集100mL氢气所需时间 |
| ① |
薄片 |
15 |
200 |
| ② |
薄片 |
25 |
90 |
| ③ |
粉末 |
25 |
10 |
(1)该实验的目的是研究、对锌和稀盐酸反应速率的影响。
(2)实验①和②表明;
(3)能表明固体的表面积对反应速率影响的实验编号是和。
(4)要加快该反应速率,除了上述表中的因素外,你试举出两条。