已知 在水溶液中存在平衡:
在水溶液中存在平衡: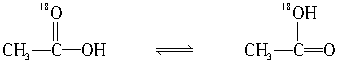 。
。 与CH3CH2OH酯化时,不可能生成的是( )
与CH3CH2OH酯化时,不可能生成的是( )
A.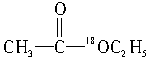 |
B. |
| C.H—18OH |
| D.H2O |
已知在25℃、1.0×105Pa条件下,2mol氢气燃烧生成水蒸气放出484 kJ热量。下列热化学方程式正确的是
| A.H2O(g)= H2(g)+1/2 O2(g)△H=+242 kJ·mol-1 |
| B.2H2(g)+O2(g) = 2H2O(l)△H=-484 kJ·mol-1 |
| C.H2(g)+1/2 O2(g)= H2O(g)△H=+242 kJ·mol-1 |
| D.2H2(g)+O2(g)= 2H2O(g)△H=+484 kJ·mol-1 |
下列变化完全符合右图图示的是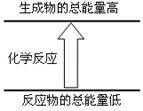
①液态水汽化 ②将胆矾加热变为白色粉末 ③浓硫酸稀释 ④生石灰溶于水
⑤二氧化碳与灼热的碳反应 ⑥碘的升华 ⑦Ba(OH)2·8H2O与NH4Cl反应
| A.①②⑥ | B.②⑤⑦ | C.①②⑤⑥⑦ | D.②④⑤⑦ |
下列说法中不正确的是
| A.19世纪中叶,门捷列夫的突出贡献是发现元素周期律 |
| B.在金属和非金属元素交界处最容易找到半导体材料 |
| C.在过渡元素中容易找到各种优良的催化剂和耐高温、耐腐蚀的合金材料 |
| D.根据硼在元素周期表中的位置,推测硼的最高价含氧酸的化学式可能是HBO3 |
常温下,分别将四块形状相同,质量为7 g的铁块同时投入下列四种溶液中,生成氢气速率最快的是
| A.200 mL 2 mol·L-1 HCl | B.100 mL 2 mol·L-1 H2SO4 |
| C.100 mL 3 mol·L-1 HCl | D.50 mL 18.4 mol·L-1 H2SO4 |
下列叙述中正确的是
| A.最外层为2个电子的原子都是金属原子 |
| B.电子能量越低,其运动区域离核越近 |
| C.每个电子层作为最外层时,最多可容纳的电子数均为8 |
| D.从Li到F、从Na到Cl,元素的最高正化合价均呈现从+1到+7价的变化 |