分子式为C5H11Cl的有机物,分子中有两个—CH3,两个—CH2—,一个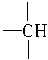 和一个—Cl,该物质的结构有( )
和一个—Cl,该物质的结构有( )
| A.2种 | B.3种 | C.4种 | D.5种 |
氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于阴影部分的是( )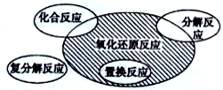
| A.Cl2+2KBr=Br2+2KCl |
B.2NaHCO3  Na2CO3+H2O+CO2↑ Na2CO3+H2O+CO2↑ |
| C.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| D.2Na2O2+2CO2=2Na2CO3+O2 |
实验室中以下物质的贮存方法不正确的是()
| A.少量液溴可用水封存,防止溴挥发 |
| B.少量金属钠保存在煤油中 |
| C.浓硝酸用带橡胶塞的细口、棕色试剂瓶盛放,并贮存在阴凉处 |
| D.保存硫酸亚铁溶液时,要向其中加入少量硫酸和铁粉 |
下图是某燃煤发电厂处理废气的装置示意图。装置内发生的主要反应中不含()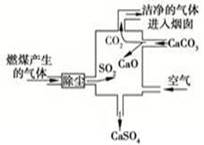
| A.化合反应 | B.分解反应 |
| C.置换反应 | D.氧化还原反应 |
分类是化学学习和研究的常用手段。下列分类依据和结论都正确的是()。
| A.HClO、HNO3、浓H2SO4都具强氧化性,都是氧化性酸 |
| B.H2O、HCOOH、Cu2(OH)2CO3均含有氧元素,都是氧化物 |
| C.HF、CH3COOH、CH3CH2OH都易溶于水,都是电解质 |
| D.HCOOH、H2CO3、H2SO4分子中均含有两个氢原子,都是二元酸 |
合成氨工业、硫酸工业的生产工艺流程大致为:
合成塔和接触室中的反应分别为:N2(g)+3H2(g)  2NH3(g)△H﹤0; 2SO2(g)+O2(g)
2NH3(g)△H﹤0; 2SO2(g)+O2(g)  2SO3(g)△H﹤0
2SO3(g)△H﹤0
(1)写出流程中设备的名称:B,X。
(2)进入合成塔和接触室中的气体都要进行热处理,最理想的热处理方法是。
(3)采用循环操作可提高原料的利用率,下列生产中,采用循环操作的是(填序号)。
①硫酸工业②合成氨工业③硝酸工业
(4)工业上常用98.3%的浓硫酸吸收SO3而不用稀硫酸或水的原因是。
(5)工业生产中常用氨——酸法进行尾气脱硫,以达到消除污染、废物利用的目的。硫酸工业尾气中的SO2经处理可以得到一种化肥,该肥料的化学式是。